Examen QIR 2025 Resuelto
Recopilación completa de preguntas con respuestas comentadas y explicaciones detalladas.
Pregunta 1
¿Cuál de las siguientes fórmulas se denomina con el nombre común de cinabrio?:
- 1. PbS.
- 2. HgS.
- 3. ZnS.
- 4. Sb2S3.
Explicación:
El cinabrio es un mineral de la clase de los sulfuros, compuesto en un 85% por mercurio y un 15% de azufre.- • Sulfuro de Mercurio (II) (Respuesta Correcta): La fórmula química del cinabrio es HgS. Es la principal mena de la que se extrae el mercurio elemental y es conocido históricamente por su color rojo intenso, habiéndose utilizado como pigmento (bermellón) desde la antigüedad.
- • Otros sulfuros comunes:– PbS: Galena (mena de plomo).- ZnS: Esfalerita o Blenda de zinc.- Sb2S3: Estibina o Antimonita (mena de antimonio).
Pregunta 2
¿Por qué NO se recomienda consumir en exceso aguas minerales ricas en magnesio?:
- 1. Porque el magnesio puede interferir con la absorción intestinal de sodio.
- 2. Porque el exceso de ion magnesio puede producir efecto laxante.
- 3. Porque el magnesio reduce la acidez gástrica en exceso.
- 4. Porque el magnesio se deposita en tejidos blandos y forma cálculos.
Explicación:
El magnesio es un catión divalente que, en concentraciones elevadas dentro de la luz intestinal, presenta propiedades farmacodinámicas específicas sobre el tránsito digestivo.- • Efecto Osmótico (Respuesta Correcta): Las sales de magnesio son poco absorbibles en el intestino. Al permanecer en la luz intestinal, actúan por ósmosis reteniendo agua, lo que aumenta el volumen del contenido fecal y estimula el peristaltismo. Este es el motivo por el cual el exceso de ion magnesio produce un efecto laxante, pudiendo derivar en diarreas osmóticas.
- • Aplicación clínica: Este principio es el mismo que se utiliza en preparados farmacéuticos como la «leche de magnesia» o las sales de Epsom para el tratamiento del estreñimiento ocasional.
Pregunta 3
¿Cómo varía el potencial de ionización en la Tabla Periódica?:
- 1. Es directamente proporcional a la carga nuclear efectiva.
- 2. Es inversamente proporcional a la carga nuclear efectiva.
- 3. Es cuadráticamente proporcional a la carga nuclear efectiva.
- 4. No guarda ninguna relación con la variación de la carga nuclear efectiva.
Explicación:
El Potencial de Ionización (PI) depende de la fuerza con la que el núcleo atrae al electrón más externo. Según el modelo mecanocuántico aproximado (similar al de Bohr), la energía es proporcional a:
PI ∝ Zeff2 / n2
- • Análisis de la proporcionalidad:
- – La relación matemática incluye el término Zeff al cuadrado, no linealmente, lo que cuestiona la opción 1 («directamente proporcional»).
- – Además, la relación ignora la variable crítica n (número cuántico principal).
- – Al bajar en un grupo, Zeff aumenta ligeramente, pero el PI disminuye drásticamente debido al aumento de n (mayor distancia). Esto contradice la afirmación de que el PI es directamente proporcional a Zeff en toda la tabla.
- • Causa de la Impugnación: Ninguna de las opciones describe correctamente la variación global. La opción 1 es una simplificación válida solo para un periodo (donde n es constante), pero falsa para un grupo. La opción 3 es matemáticamente más precisa respecto a Zeff pero incompleta al faltar n.
Pregunta 4
¿Cómo es la molécula de ozono?:
- 1. Lineal, con dos enlaces sencillos.
- 2. Lineal, con dos enlaces dobles.
- 3. Angular, con dos formas resonantes, y orden de enlace 1,5.
- 4. Angular, con tres formas resonantes, y orden de enlace 1,33.
Explicación:
La estructura de la molécula de ozono (O3) se explica mediante la geometría molecular y el concepto de resonancia para describir la deslocalización electrónica.- • Geometría y Resonancia (Respuesta Correcta): El átomo central de oxígeno tiene una hibridación sp2 con un par de electrones no compartidos, lo que confiere a la molécula una geometría angular. Para representar correctamente sus enlaces, se utilizan dos formas resonantes donde el enlace doble se alterna entre los dos oxígenos terminales.
- • Orden de enlace: Debido a esta resonancia, los dos enlaces son idénticos y tienen una longitud intermedia entre un enlace sencillo y uno doble. El cálculo del orden de enlace resulta en 1,5 (3 pares de electrones de enlace repartidos entre 2 posiciones de enlace).
Pregunta 5
¿Cuál de estos compuestos es un excelente ácido de Lewis?:
- 1. HCl.
- 2. BCl3.
- 3. HClO2.
- 4. SiO2.
Explicación:
Según la definición de Lewis, un ácido es cualquier especie química capaz de aceptar un par de electrones solitarios de otra molécula para formar un enlace covalente.- • Deficiencia de electrones (Respuesta Correcta): El BCl3 (tricloruro de boro) es un ejemplo clásico de ácido de Lewis fuerte. El átomo de boro central tiene solo seis electrones en su capa de valencia (un octeto incompleto) y posee un orbital «p» vacío, lo que le otorga una gran afinidad por aceptar un par de electrones.
- • Comparación con ácidos de Brønsted: El HCl y el HClO2 se clasifican fundamentalmente como ácidos de Brønsted-Lowry porque su reactividad principal se basa en la donación de protones (H+), mientras que el BCl3 actúa exclusivamente mediante la aceptación de pares electrónicos.
Pregunta 6
¿En qué elemento lantánido se basan diversos complejos usados como agentes de contraste en resonancia magnética?:
- 1. Praseodimio.
- 2. Neodimio.
- 3. Gadolinio.
- 4. Disprosio.
Explicación:
Los agentes de contraste utilizados en Resonancia Magnética (RM) tienen como objetivo principal mejorar la visibilidad de estructuras internas mediante la alteración de las propiedades magnéticas de los protones del agua en los tejidos.- • Propiedades Magnéticas (Respuesta Correcta): El Gadolinio (Gd) es el lantánido más utilizado debido a que su ion (Gd3+) posee siete electrones desapareados en sus orbitales 4f. Esta configuración le otorga un elevado paramagnetismo, lo que reduce los tiempos de relajación longitudinal (T1) del agua circundante, creando una señal brillante en la imagen.
- • Quelatos de Gadolinio: Debido a la toxicidad del ion libre, se administra en forma de complejos estables (quelatos), como el gadopentetato de dimeglumina, que aseguran su correcta distribución y posterior excreción renal.
Pregunta 7
¿Cuál de estos ligandos presenta isomería de enlace?:
- 1. Agua.
- 2. Amoníaco.
- 3. Etilendiamina.
- 4. Nitrito.
Explicación:
La isomería de enlace (o isomería de coordinación) ocurre en compuestos de coordinación cuando un ligando ambidentado puede unirse al átomo metálico central a través de átomos diferentes.- • Ligandos Ambidentados (Respuesta Correcta): El ion nitrito (NO2–) es un ligando ambidentado clásico. Posee dos posibles átomos dadores: puede coordinarse a través del nitrógeno (formando un complejo de tipo nitro) o a través del oxígeno (formando un complejo de tipo nitrito). Esta dualidad genera isómeros de enlace con propiedades físicas y químicas distintas.
- • Análisis de las otras opciones:– El agua (acua) y el amoníaco (ammina) son ligandos monodentados simples que solo poseen un átomo capaz de donar el par de electrones (O y N respectivamente).- La etilendiamina (en) es un ligando bidentado quelante, pero se une exclusivamente a través de sus dos átomos de nitrógeno.
Pregunta 8
¿Cuál de estas especies es inestable en agua?:
- 1. Co3+ (oxida el agua a oxígeno, reduciéndose a Co2+).
- 2. Co2+ (reduce el agua a hidrógeno, oxidándose a Co3+).
- 3. Fe3+ (oxida el agua a oxígeno, reduciéndose a Fe2+).
- 4. Fe2+ (reduce el agua a hidrógeno, oxidándose a Fe3+).
Explicación:
La estabilidad de los iones metálicos en disolución acuosa depende de su potencial estándar de reducción frente a los potenciales de oxidación y reducción del propio agua.- • Alto potencial de oxidación (Respuesta Correcta): El ion Co3+ es un oxidante extremadamente fuerte en medio acuoso (E° ≈ 1,82 V). Este valor es muy superior al potencial necesario para oxidar el agua a oxígeno (E° = 1,23 V). Por tanto, el Co3+ reacciona espontáneamente con el agua, liberando O2 y reduciéndose a la forma mucho más estable Co2+.
- • Comparación con el Hierro: Aunque el sistema Fe3+/Fe2+ tiene un potencial positivo (0,77 V), no es lo suficientemente alto como para oxidar el agua de forma termodinámicamente favorable en condiciones estándar, lo que permite que el Fe3+ sea estable en disoluciones ácidas.
Pregunta 9
El 60Co es un isótopo radiactivo muy utilizado en la terapia contra el cáncer. ¿Qué tipo de radiación presenta?:
- 1. Alfa.
- 2. Beta.
- 3. Gamma.
- 4. Emisión de positrones.
Explicación:
El Cobalto-60 (60Co) es un isótopo radiactivo sintético que se produce por activación neutrónica del cobalto estable. Su utilidad en medicina radica en la naturaleza de su desintegración energética.- • Desintegración y emisión (Respuesta Correcta): Aunque el 60Co se desintegra inicialmente mediante la emisión de una partícula beta para transformarse en un estado excitado de Níquel-60 (60Ni), este último libera inmediatamente el exceso de energía en forma de radiación gamma de alta energía (fotones de 1,17 y 1,33 MeV). En el contexto terapéutico (teleterapia de cobalto), es esta radiación gamma la que se aprovecha por su gran poder de penetración para destruir células cancerosas.
- • Uso clínico: Debido a la alta energía de sus rayos gamma, el cobalto-60 permite tratar tumores profundos, siendo una de las fuentes de radiación más fiables y utilizadas históricamente en radioterapia.
Pregunta 10
En el contexto de la teoría de Lewis, ¿qué tipo de interacción se establece cuando el amoníaco (NH3) reacciona con el trifluoruro de boro (BF3)?:
- 1. Formación de un enlace covalente por compartición equitativa de electrones.
- 2. Formación de un enlace covalente coordinado mediante donación de un par electrónico desde el nitrógeno al boro.
- 3. Formación de un enlace iónico por transferencia completa de electrones.
- 4. Formación de un enlace de hidrógeno entre el nitrógeno y el flúor.
Explicación:
La reacción entre el amoníaco y el trifluoruro de boro es el ejemplo paradigmático de una reacción ácido-base de Lewis, donde no hay transferencia de protones, sino de pares electrónicos.- • Enlace Dativo o Coordinado (Respuesta Correcta): El nitrógeno en el NH3 posee un par de electrones solitarios (base de Lewis), mientras que el boro en el BF3 tiene un orbital «p» vacío y un octeto incompleto (ácido de Lewis). Al reaccionar, el nitrógeno dona su par electrónico al boro para formar un enlace covalente coordinado, resultando en un aducto estable.
- • Cambio en la geometría: Tras la formación del enlace, el boro pasa de una hibridación sp2 (trigonal plana) a una hibridación sp3 (tetraédrica) para acomodar el nuevo par de electrones compartido.
Pregunta 11
¿Cuál de los siguientes ligandos es más probable que forme un complejo octaédrico de alto spin con el ion Co2+?:
- 1. CN⁻.
- 2. CO.
- 3. I⁻.
- 4. Etilendiamina (en).
Explicación:
La formación de complejos de bajo o alto espín depende de la magnitud del desdoblamiento del campo cristalino (Δo) que genera el ligando en comparación con la energía de apareamiento electrónico.- • Serie Espectroquímica (Respuesta Correcta): Los ligandos se clasifican según su capacidad para desdoblar los orbitales «d». El ion yoduro (I⁻) se encuentra en el extremo de campo débil de la serie espectroquímica. Al generar un desdoblamiento pequeño, la energía necesaria para aparear electrones es mayor que el salto energético entre orbitales, favoreciendo la ocupación de los orbitales superiores y dando lugar a un complejo de alto espín.
- • Comparación con el resto: El CN⁻ y el CO son ligandos de campo muy fuerte (producen bajo espín), mientras que la etilendiamina es un ligando de campo intermedio-fuerte que también tiende a favorecer el bajo espín en muchos metales de transición.
Pregunta 12
Considere la siguiente reacción redox ajustada: 16 HCl (conc) + 2 KMnO4 (s) → 5 Cl2 (g) + 2 KCl (aq) + 2 MnCl2 (aq) + 8 H2O (l)
¿Cuál de las siguientes afirmaciones es correcta respecto a los agentes redox?:- 1. MnO4– actúa como agente oxidante y el manganeso se oxida.
- 2. MnO4– actúa como agente reductor y el manganeso se reduce.
- 3. MnO4– actúa como agente reductor y el manganeso se oxida.
- 4. MnO4– actúa como agente oxidante y el manganeso se reduce.
Explicación:
Para identificar los agentes en una reacción redox, debemos analizar los cambios en los estados de oxidación de los elementos involucrados.- • Análisis del Manganeso (Respuesta Correcta): En el reactivo KMnO4 (o ion MnO4–), el manganeso tiene un estado de oxidación de +7. En los productos, forma parte del MnCl2, donde su estado de oxidación es +2. Como el estado de oxidación disminuye, el manganeso se reduce. Aquella especie que se reduce y provoca la oxidación de otra se denomina agente oxidante.
- • Análisis del Cloro: El cloro pasa de -1 en el HCl a 0 en el Cl2 gaseoso. Por lo tanto, el cloro se oxida, actuando el HCl como el agente reductor de la reacción.
Pregunta 13
¿Cuál de los siguientes complejos puede presentar isomería geométrica (cis/trans)?:
- 1. [Pt(NH3)Br3]⁻.
- 2. [Fe(CN)6]³⁻.
- 3. [Pt(NH3)3Cl]⁺.
- 4. [Co(H2O)4Cl2]⁺.
Explicación:
La isomería geométrica (cis/trans) aparece cuando los ligandos pueden ocupar posiciones relativas distintas (adyacentes o opuestas) en la esfera de coordinación del metal.- • Complejos Octaédricos (Respuesta Correcta): El ion [Co(H2O)4Cl2]⁺ es un complejo octaédrico de tipo [MA4B2]. En esta configuración, los dos ligandos cloruro (B) pueden situarse en vértices adyacentes del octaedro (isómero cis, ángulo de 90°) o en vértices opuestos (isómero trans, ángulo de 180°).
- • Análisis de las otras opciones:– [Pt(NH3)Br3]⁻ y [Pt(NH3)3Cl]⁺ son complejos plano-cuadrados de tipo [MA3B]. Al tener tres ligandos iguales, cualquier posición que ocupe el cuarto ligando es equivalente, por lo que no presentan isomería geométrica.- [Fe(CN)6]³⁻ es un complejo homoléptico (todos los ligandos son iguales), por lo que es imposible que presente isómeros geométricos.
Pregunta 14
¿Cuál es el origen del color en el rubí?:
- 1. Pequeñas cantidades de Cr3+ sustituyendo a Al3+ en posiciones octaédricas de cristales de corindón.
- 2. Pequeñas cantidades de Fe3+ sustituyendo a Al3+ en posiciones octaédricas de cristales de corindón.
- 3. Pequeñas cantidades de Cr3+ sustituyendo a Al3+ en posiciones tetraédricas de cristales de corindón.
- 4. Pequeñas cantidades de Fe3+ sustituyendo a Al3+ en posiciones tetraédricas de cristales de corindón.
Explicación:
El rubí es una variedad del mineral corindón (Al2O3) cuya coloración característica se debe a la presencia de impurezas de metales de transición que actúan como centros de color.- • Sustitución Isomórfica (Respuesta Correcta): El color rojo intenso del rubí se origina cuando iones de Cromo (Cr3+) sustituyen a una pequeña fracción de los iones de aluminio (Al3+). En la red del corindón, el aluminio ocupa posiciones octaédricas.
- • Transiciones d-d: Al estar el Cr3+ (configuración d3) en un campo de ligandos octaédrico rodeado de oxígenos, se produce un desdoblamiento de los orbitales «d». La absorción de luz verde y azul para promover electrones entre estos niveles deja pasar la luz roja, que es la que percibimos.
Pregunta 15
¿Cuál de estas definiciones corresponde a la wurtzita?:
- 1. Empaquetamiento cúbico compacto con todos los huecos octaédricos ocupados.
- 2. Empaquetamiento cúbico compacto con la mitad de los huecos octaédricos ocupados.
- 3. Empaquetamiento hexagonal compacto con todos los huecos tetraédricos ocupados.
- 4. Empaquetamiento hexagonal compacto con la mitad de los huecos tetraédricos ocupados.
Explicación:
La wurtzita es una de las formas cristalinas del sulfuro de zinc (ZnS). Su estructura se describe habitualmente considerando un empaquetamiento de aniones donde los cationes ocupan determinados huecos intersticiales.- • Estructura Cristalina (Respuesta Correcta): La wurtzita presenta un empaquetamiento hexagonal compacto (hcp) de iones sulfuro (S2-). En este tipo de empaquetamiento, existen dos huecos tetraédricos por cada átomo del empaquetamiento. Para mantener la estequiometría 1:1 del ZnS, los iones de zinc (Zn2+) ocupan la mitad de los huecos tetraédricos disponibles.
- • Diferencia con la Blenda de Zinc: Mientras que la wurtzita se basa en un empaquetamiento hexagonal, la blenda de zinc (la otra forma del ZnS) se basa en un empaquetamiento cúbico compacto (fcc), ocupando también la mitad de los huecos tetraédricos.
Pregunta 16
Indique cuál de estas afirmaciones respecto a la ecuación de Langmuir es VERDADERA:
- 1. Se utiliza para procesos de adsorción de gases o líquidos en un sólido.
- 2. Asume la adsorción de moléculas en multicapas.
- 3. Hace referencia a procesos de adsorción no isotérmicos.
- 4. Es independiente de la velocidad de desorción.
Explicación:
La isoterma de Langmuir es el modelo más sencillo y fundamental para describir la adsorción química y física en superficies sólidas.- • Ámbito de aplicación (Respuesta Correcta): La ecuación de Langmuir describe cómo se distribuyen las moléculas de una fase fluida (ya sea un gas o un líquido) al adherirse a la superficie de un sólido (el adsorbente). Es la base para entender procesos de catálisis y purificación.
- • Suposiciones del modelo:– Contrario a la opción 2, el modelo asume monocapas (las moléculas no se apilan unas sobre otras).- Contrario a la opción 3, se refiere a procesos isotérmicos (la temperatura se mantiene constante).- Contrario a la opción 4, la isoterma se deriva precisamente del equilibrio dinámico entre la velocidad de adsorción y la velocidad de desorción.
Pregunta 17
En los espectros electrónicos de moléculas diatómicas, ¿cuándo una transición electrónica está permitida?:
- 1. Cuando cambia el espín total del sistema.
- 2. Cuando el momento angular orbital cambia en 0 ó ±1 y el espín total no cambia.
- 3. Cuando ambos estados tienen la misma paridad (g → g o u → u).
- 4. Cuando el momento angular orbital cambia en ±2.
Explicación:
Las transiciones electrónicas en moléculas están gobernadas por reglas de selección que determinan si una transición es probable (permitida) o improbable (prohibida) ante la radiación.- • Reglas de Selección (Respuesta Correcta): Para que una transición se considere permitida por dipolo eléctrico, debe cumplir con:1. Regla del Espín: El espín total no debe variar (ΔS = 0). Esto significa que no hay cambio en la multiplicidad de los estados.2. Regla del Momento Angular: El componente del momento angular orbital (representado por Λ) solo puede cambiar en 0 o ±1.
- • Regla de Paridad: En moléculas con centro de inversión, la regla de Laporte dicta que solo se permiten transiciones entre estados de distinta paridad (de g a u, o de u a g). Por ello, la opción 3 (misma paridad) es incorrecta.
Pregunta 18
La reacción de ionización del H3PO4 sucede en 3 etapas. ¿Cuál de las constantes de ionización es mayor?:
- 1. La de la primera etapa.
- 2. La de la segunda etapa.
- 3. La de la tercera etapa.
- 4. Las constantes para las 3 etapas son iguales.
Explicación:
El ácido fosfórico (H3PO4) es un ácido poliprótico, lo que significa que puede ceder más de un protón en etapas sucesivas, cada una con su propia constante de acidez (Ka1, Ka2 y Ka3).- • Fuerza de ionización (Respuesta Correcta): En todos los ácidos polipróticos, la constante de la primera etapa (Ka1) es siempre significativamente mayor que las siguientes. Esto se debe a que es mucho más fácil retirar un protón (H+) de una molécula neutra que de un ion con carga negativa, ya que la atracción electrostática retiene con más fuerza a los protones restantes conforme aumenta la carga negativa del anión.
- • Valores comparativos: Para el H3PO4, los valores aproximados son Ka1 ≈ 7,5 × 10⁻³, Ka2 ≈ 6,2 × 10⁻⁸ y Ka3 ≈ 4,2 × 10⁻¹³. La diferencia entre cada etapa suele ser de varios órdenes de magnitud.
Pregunta 19
Indique para qué catión M2+ se espera una entalpía de hidratación superior a la correspondiente a su tamaño catiónico:
- 1. Ca2+.
- 2. Mn2+.
- 3. Cu2+.
- 4. Zn2+.
Explicación:
La entalpía de hidratación depende principalmente de la relación carga/radio del ion. Sin embargo, en los metales de transición, aparece una contribución adicional debida a la Teoría del Campo Cristalino.- • Energía de Estabilización del Campo Cristalino (EECC): Los cationes con orbitales «d» parcialmente llenos experimentan una estabilización extra al coordinarse con moléculas de agua (ligandos). Esta energía adicional hace que la entalpía de hidratación sea más negativa (superior en valor absoluto) de lo que predeciría el modelo puramente electrostático basado en el tamaño.
- • Análisis del Cu2+ (Respuesta Correcta): El cobre(II) es un sistema d9. Presenta una EECC significativa y, además, experimenta una fuerte distorsión de Jahn-Teller, lo que estabiliza aún más el complejo acuoso [Cu(H2O)6]2+, aumentando la entalpía por encima de la tendencia esperada.
- • Otros casos: El Ca2+ (d0), el Mn2+ (d5 alto espín) y el Zn2+ (d10) tienen una EECC de cero. Por tanto, sus entalpías de hidratación se ajustan casi perfectamente a lo esperado únicamente por su radio iónico, sin presentar ese «extra» de estabilidad.
Pregunta 20
Dadas las siguientes especies: NaI, NH3, HF, H2O y BaO. Indique el orden correcto según el punto de ebullición:
- 1. H2O > HF > NH3 > NaI > BaO.
- 2. BaO > NaI > HF > H2O > NH3.
- 3. BaO > NaI > NH3 > H2O > HF.
- 4. BaO > NaI > H2O > HF > NH3.
Explicación:
El punto de ebullición de una sustancia depende de la intensidad de las fuerzas intermoleculares o de la energía de red que mantiene unidas a sus unidades constituyentes.- • Compuestos Iónicos (Máximos puntos de ebullición): El BaO y el NaI son sólidos iónicos con puntos de ebullición muy elevados debido a las fuertes atracciones electrostáticas. Entre ellos, el BaO tiene un punto mayor que el NaI porque sus iones tienen mayor carga (Ba2+, O2- frente a Na+, I–), lo que resulta en una energía reticular mucho más alta.
- • Enlaces de Hidrógeno (Compuestos moleculares): El H2O, el HF y el NH3 presentan puentes de hidrógeno, pero su intensidad varía:- El H2O tiene el punto más alto de los tres porque puede formar, en promedio, cuatro puentes de hidrógeno por molécula.- El HF sigue al agua; aunque el flúor es más electronegativo, solo puede formar dos puentes de hidrógeno por molécula.- El NH3 tiene el punto más bajo debido a que el nitrógeno es menos electronegativo y la intensidad de sus enlaces de hidrógeno es menor.
Pregunta 21
¿Cuántos electrones desapareados tiene el catión Fe3+?:
- 1. 2.
- 2. 3.
- 3. 4.
- 4. 5.
Explicación:
Para determinar el número de electrones desapareados, debemos escribir la configuración electrónica del átomo neutro y luego retirar los electrones necesarios para formar el catión.- • Configuración del Hierro (Z=26): El estado fundamental del Fe neutro es [Ar] 3d6 4s2.
- • Formación del catión Fe3+ (Respuesta Correcta): Al ionizarse, el hierro pierde primero los 2 electrones del orbital 4s y después 1 electrón del orbital 3d. La configuración resultante es [Ar] 3d5.
- • Regla de Hund: Según la regla de máxima multiplicidad de Hund, los 5 electrones ocupan los cinco orbitales «d» de forma individual (paralela) antes de empezar a aparearse. Por tanto, el ion Fe3+ presenta 5 electrones desapareados.
Pregunta 22
¿Cómo se define la polarización iónica de un material dieléctrico homogéneo?:
- 1. Como la polarización debida a los desplazamientos de cargas positivas respecto a las negativas.
- 2. Como el desplazamiento de los iones de sus posiciones de equilibrio.
- 3. Como la orientación de dipolos en la dirección del campo eléctrico.
- 4. Como la acumulación de cargas libres en la superficie de materiales cristalinos.
Explicación:
La polarización en materiales dieléctricos se refiere al desplazamiento relativo de cargas bajo la influencia de un campo eléctrico externo. Existen distintos mecanismos dependiendo de la naturaleza del material.- • Polarización Iónica (Respuesta Correcta): Este mecanismo es característico de los sólidos iónicos. Al aplicar un campo eléctrico, los cationes son atraídos en la dirección del campo y los aniones en sentido opuesto. Esto provoca un desplazamiento de los iones de sus posiciones de equilibrio en la red cristalina, generando un momento dipolar neto en el material.
- • Otros mecanismos:– La polarización electrónica (opción 1) se refiere al desplazamiento de la nube de electrones respecto al núcleo.- La polarización de orientación (opción 3) ocurre en materiales con dipolos permanentes que se alinean con el campo.- La polarización de carga espacial (relacionada con la opción 4) implica la acumulación de portadores de carga en interfaces o defectos.
Pregunta 23
¿Qué forma geométrica tiene la molécula de CO2?:
- 1. Plana triangular.
- 2. Pirámide triangular.
- 3. Lineal.
- 4. Tetraédrica.
Explicación:
La geometría de la molécula de dióxido de carbono (CO2) se predice mediante la Teoría de Repulsión de Pares de Electrones de la Capa de Valencia (VSEPR) y la hibridación de sus orbitales.- • Hibridación del átomo central (Respuesta Correcta): El átomo de carbono central se une a dos átomos de oxígeno mediante dos enlaces dobles. Para minimizar la repulsión entre estos dos grupos de electrones (regiones de alta densidad electrónica), el carbono adopta una hibridación sp.
- • Disposición espacial: Los dos orbitales híbridos sp se orientan en direcciones opuestas formando un ángulo de 180°, lo que confiere a la molécula una geometría lineal. Debido a esta simetría, aunque los enlaces C-O son polares, los momentos dipolares se anulan, resultando en una molécula apolar.
Pregunta 24
¿Cuál de estos postulados NO es aplicable a la teoría de orbitales moleculares?:
- 1. Los orbitales moleculares se definen matemáticamente por combinación lineal de orbitales atómicos.
- 2. Un orbital molecular está completo si contiene dos electrones.
- 3. De la combinación lineal de un determinado número de orbitales atómicos se obtiene el mismo número de orbitales moleculares.
- 4. Los orbitales moleculares llamados enlazantes son los que se encuentran en mayor número y tienen una energía mayor que los orbitales atómicos de los que proceden.
Explicación:
La Teoría de Orbitales Moleculares (TOM) describe la estructura electrónica de las moléculas considerando que los electrones se mueven en orbitales que se extienden por toda la molécula.- • Orbitales Enlazantes vs Antienlazantes (Respuesta Correcta): El postulado 4 es falso porque los orbitales enlazantes tienen siempre una energía menor que los orbitales atómicos de partida (lo que confiere estabilidad a la molécula). Además, en una combinación binaria, se produce el mismo número de orbitales enlazantes que antienlazantes; los que tienen mayor energía que los orbitales atómicos son los llamados antienlazantes.
- • Análisis de los postulados correctos:– El método LCAO (Combinación Lineal de Orbitales Atómicos) es la base matemática de la teoría (Opción 1).- Al igual que los atómicos, los moleculares siguen el principio de exclusión de Pauli: máximo dos electrones con espines opuestos (Opción 2).- Se cumple siempre la conservación del número de orbitales: si combinamos n orbitales atómicos, obtendremos n orbitales moleculares (Opción 3).
Pregunta 25
¿Cómo se denominan los sólidos con una gran fuerza de cohesión entre las partículas que los componen, las cuales hacen que se distribuyan de forma regular y simétrica en el espacio en forma de redes?:
- 1. Sólidos cristalinos o cristales.
- 2. Sólidos amorfos.
- 3. Vidrios.
- 4. Cristales líquidos.
Explicación:
El estado sólido se caracteriza por tener una forma y volumen propios debido a las intensas fuerzas de atracción entre sus constituyentes (átomos, iones o moléculas).- • Orden de Largo Alcance (Respuesta Correcta): Los sólidos cristalinos son aquellos en los que las partículas se sitúan siguiendo un patrón repetitivo tridimensional, denominado red cristalina. Esta organización regular y simétrica es consecuencia directa de la maximización de las fuerzas de cohesión, resultando en estructuras estables con puntos de fusión definidos.
- • Diferenciación con otros estados:– Los sólidos amorfos (como los vidrios) carecen de este ordenamiento periódico; sus partículas están distribuidas de forma desordenada o solo con orden de corto alcance.- Los cristales líquidos presentan propiedades intermedias entre los líquidos y los sólidos, manteniendo cierto orden de orientación pero con fluidez.
Pregunta 26
¿Qué tipo de información NO se puede obtener de un material mediante microscopía electrónica?:
- 1. Estudio de la microestructura por medio de la obtención de imágenes.
- 2. Estudio de los distintos grupos funcionales superficiales presentes en el material.
- 3. Determinación del grado de cristalinidad de la muestra.
- 4. Microanálisis in situ.
Explicación:
La microscopía electrónica (tanto de barrido SEM como de transmisión TEM) utiliza un haz de electrones para interactuar con la muestra, generando señales que informan sobre su topografía, morfología y composición elemental.- • Limitaciones químicas (Respuesta Correcta): Aunque la microscopía electrónica puede identificar qué elementos están presentes (mediante detectores de rayos X o EDX), no proporciona información sobre cómo están enlazados esos átomos. Para identificar grupos funcionales (como alcoholes, cetonas, aminas, etc.), se requieren técnicas espectroscópicas que analicen las vibraciones moleculares o los estados de enlace, como la espectroscopía infrarroja (FTIR) o la espectroscopía de fotoelectrones emitidos por rayos X (XPS).
- • Capacidades de la técnica:– Sí permite ver la microestructura (granos, poros, defectos) con gran resolución.- Sí permite estudiar la cristalinidad mediante patrones de difracción de electrones.- Sí permite el microanálisis elemental puntual sobre la superficie.
Pregunta 27
¿Cómo se define el enlace metálico?:
- 1. Enlaces entre átomos de los grupos 1 y 2 de la tabla periódica.
- 2. Enlace donde los electrones se comparten entre 2 átomos.
- 3. Enlace donde la deslocalización de electrones se extiende sobre un número enorme de átomos.
- 4. Enlace de atracción electrostática entre iones.
Explicación:
El enlace metálico es el modelo que explica la cohesión y las propiedades características (como la conductividad) de los metales.- • Modelo del «Mar de Electrones» (Respuesta Correcta): En un metal, los átomos pierden sus electrones de valencia, convirtiéndose en una red de iones positivos (cationes). Estos electrones liberados no pertenecen a ningún átomo en particular ni se comparten solo entre pares vecinos (como en el enlace covalente), sino que están deslocalizados y se mueven libremente a través de toda la estructura cristalina, actuando como un «pegamento» electrostático que mantiene unidos a los cationes.
- • Diferencia con otros enlaces:– La opción 2 describe el enlace covalente (compartición localizada).- La opción 4 describe el enlace iónico (atracción electrostática entre cargas opuestas fijas).
Pregunta 28
¿Qué gases se obtienen en la reacción de “gas de agua”?:
- 1. CO2 y O2.
- 2. H2 y O2.
- 3. H2 y CO.
- 4. H2 y N2.
Explicación:
La reacción del «gas de agua» es un método industrial clásico para obtener combustible gaseoso a partir de carbón y agua.- • Proceso Químico (Respuesta Correcta): Se hace pasar vapor de agua sobre coque (carbón) al rojo vivo (a altas temperaturas, típicamente >1000 °C). La reacción es endotérmica y se representa como:
C (s) + H2O (g) → CO (g) + H2 (g) El producto es una mezcla de monóxido de carbono (CO) e hidrógeno (H2), conocida comúnmente como «gas de síntesis» o «gas de agua». - • Usos: Esta mezcla es muy valiosa porque el hidrógeno es un combustible limpio y el monóxido de carbono es un reactivo clave para la síntesis de otros compuestos orgánicos (como metanol).
Pregunta 29
¿Cuál de los siguientes compuestos presenta estructura tipo perovskita?:
- 1. NaCl.
- 2. ZnS.
- 3. CaF2.
- 4. CaTiO3.
Explicación:
La estructura de perovskita es una de las disposiciones cristalinas más importantes en química del estado sólido y ciencia de materiales, caracterizada por la fórmula general ABX3.- • Mineral Perovskita (Respuesta Correcta): El titanato de calcio (CaTiO3) es el mineral que da nombre a toda esta familia estructural. En su celda unidad ideal:- El catión Ti4+ (catión B, más pequeño) ocupa el centro del cubo con coordinación octaédrica.- El catión Ca2+ (catión A, más grande) ocupa los vértices del cubo con coordinación 12.- Los aniones O2- (anión X) se sitúan en los centros de las caras.
- • Descarte de opciones:– NaCl: Estructura tipo sal gema (halita), estequiometría 1:1.- ZnS: Estructura tipo blenda o wurtzita, estequiometría 1:1.- CaF2: Estructura tipo fluorita, estequiometría 1:2.
Pregunta 30
¿Cuál de las siguientes afirmaciones describe la reacción ácido-base dura blanda según el principio de ácidos y bases duros y blandos de Pearson (HSAB)?:
- 1. Tendencia de ácidos duros a interactuar con bases duras.
- 2. Neutralización exclusiva entre ácidos y bases de igual carga.
- 3. Tendencia de ácidos blandos a interactuar con bases duras.
- 4. Reacción con condicionamiento exclusivamente termodinámico sin componente cinético.
Explicación:
El principio HSAB (Hard and Soft Acids and Bases), propuesto por Ralph Pearson, es una regla cualitativa utilizada para predecir la estabilidad de los complejos metálicos y los mecanismos de reacción.- • La Regla Fundamental (Respuesta Correcta): El principio establece que «lo semejante prefiere a lo semejante».- Los ácidos duros (pequeños, alta carga, baja polarizabilidad) se unen más fuertemente a bases duras. Esta interacción es predominantemente iónica o electrostática.- Los ácidos blandos (grandes, baja carga, alta polarizabilidad) se unen más fuertemente a bases blandas. Esta interacción tiene un carácter marcadamente covalente.
- • Incompatibilidad: La interacción cruzada (ácido duro con base blanda o viceversa) es desfavorable y conduce a complejos menos estables, lo que invalida la opción 3.
Pregunta 31
En un complejo octaédrico d6 de campo fuerte, ¿cuál es la configuración electrónica t2g/eg correcta?:
- 1. t2g4 eg2.
- 2. t2g3 eg3.
- 3. t2g6 eg0.
- 4. t2g2 eg4.
Explicación:
Según la Teoría del Campo Cristalino, en un entorno octaédrico, los cinco orbitales «d» se desdoblan en dos niveles de energía: un nivel inferior (t2g) y un nivel superior (eg).- • Campo Fuerte vs. Campo Débil: Un ligando de «campo fuerte» provoca un gran desdoblamiento energético (Δo) entre los niveles. Esto significa que la energía necesaria para promocionar un electrón al nivel superior eg es mayor que la energía necesaria para aparearlo en el nivel inferior t2g (Energía de apareamiento, P).
- • Configuración de Bajo Espín (Respuesta Correcta): Para un ion d6 en campo fuerte (Δo > P), los electrones prefieren ocupar y aparearse en los orbitales de menor energía antes que subir.1. Los primeros 3 electrones ocupan los orbitales t2g.2. Los siguientes 3 electrones, debido al gran salto energético, se aparean en esos mismos orbitales t2g.El resultado es que el nivel t2g se llena completamente con 6 electrones y el nivel eg permanece vacío.
Pregunta 32
En el diagrama Fe–Fe3C, la perlita es una mezcla de:
- 1. Ferrita y martensita.
- 2. Ferrita y cementita.
- 3. Austenita y grafito.
- 4. Ferrita y austenita.
Explicación:
En el diagrama de fases Hierro-Carbono (o más precisamente, Hierro-Cementita), la perlita es un microconstituyente fundamental que aparece en los aceros.- • Reacción Eutectoide (Respuesta Correcta): La perlita se forma cuando la austenita (fase γ) con un contenido de carbono del 0,77% se enfría lentamente por debajo de la temperatura eutectoide (727 °C). En este punto, la austenita se descompone simultáneamente en dos nuevas fases sólidas:1. Ferrita (α): Hierro casi puro, blando y dúctil.2. Cementita (Fe3C): Carburo de hierro, duro y frágil.
- • Estructura: Esta mezcla mecánica adopta una morfología laminar característica, alternando capas finas de ferrita y cementita, lo que le da un aspecto similar al nácar (de ahí su nombre «perlita») bajo el microscopio.
Pregunta 33
La fractura dúctil se caracteriza por:
- 1. Superficie plana y brillante.
- 2. Superficies de descohesión y clivaje.
- 3. Propagación rápida y catastrófica.
- 4. Presencia de “copa y cono”.
Explicación:
El modo en que un material se rompe ofrece información crucial sobre su comportamiento mecánico y las causas del fallo.- • Morfología «Copa y Cono» (Respuesta Correcta): La fractura dúctil ocurre tras una deformación plástica considerable. En un ensayo de tracción, el material empieza a estrecharse (formación de cuello o estricción). Se generan microhuecos en el centro que coalescen y la ruptura final ocurre por cizalladura en los bordes (a 45°), creando una forma característica donde una pieza parece una copa y la otra un cono que encaja en ella. Su superficie suele ser mate y fibrosa.
- • Fractura Frágil (Otras opciones):– Las superficies planas, brillantes y el mecanismo de «clivaje» (separación a través de planos cristalográficos específicos) son típicos de materiales frágiles (opciones 1 y 2).- La propagación rápida y catastrófica sin aviso previo (sin deformación) también define la fractura frágil (opción 3). La dúctil, en cambio, es lenta y estable.
Pregunta 34
Justifica por qué la siguiente reacción no puede producirse en el sentido en que está escrita: 2F– (ac) + 2 Cl– (ac) → F2 (g) + Cl2 (g)
Datos: Eº Cl2/Cl– = 1,358 V; Eº F2/F– = 2,87 V.- 1. Porque el F2 es más oxidante que el Cl2.
- 2. Porque el Cl2 es más oxidante que el F2.
- 3. Porque ocurren dos oxidaciones.
- 4. Porque ocurren dos reducciones.
Explicación:
Para que una reacción redox sea viable (independientemente de su espontaneidad termodinámica), debe cumplir el principio básico de conservación de la carga: debe haber una transferencia de electrones, lo que implica que una especie se oxida (pierde electrones) y otra se reduce (gana electrones) simultáneamente.- • Análisis de los estados de oxidación (Respuesta Correcta):– El ión fluoruro (F–) pasa a flúor elemental (F2): El estado de oxidación cambia de -1 a 0. Esto es una oxidación.- El ión cloruro (Cl–) pasa a cloro elemental (Cl2): El estado de oxidación cambia de -1 a 0. Esto también es una oxidación.
- • El error conceptual: La ecuación propuesta implica que ambas especies pierden electrones, pero no hay ninguna especie que los acepte. Una reacción química no puede consistir en dos semirreacciones del mismo tipo; falta el agente oxidante que se reduzca.
Pregunta 35
En relación a los compuestos de oxígeno se puede afirmar:
- 1. Los óxidos de xenón son explosivos incluso a bajas temperaturas.
- 2. Li2O y MgO son óxidos covalentes.
- 3. SiO2 es un óxido iónico.
- 4. El BeO no es un óxido anfótero.
Explicación:
Analicemos la naturaleza de los enlaces y la estabilidad de los óxidos presentados:- • Óxidos de Gases Nobles (Respuesta Correcta): El xenón, aunque es un gas noble, puede formar compuestos con oxígeno como el XeO3 (trióxido de xenón) y el XeO4 (tetróxido de xenón). Estos compuestos son termodinámicamente muy inestables (tienen una entalpía de formación muy positiva) y son oxidantes extremadamente fuertes. El XeO3 sólido es un explosivo peligroso y sensible al choque, incluso a temperatura ambiente o bajas temperaturas.
- • Análisis de las otras opciones:– Opción 2: El Li2O y el MgO están formados por metales muy electropositivos y oxígeno, por lo que son típicamente iónicos, no covalentes.- Opción 3: El SiO2 (sílice) forma una red covalente gigante, no es un compuesto iónico.- Opción 4: El BeO es uno de los ejemplos clásicos de óxido anfótero; reacciona tanto con ácidos como con bases, debido al pequeño tamaño y alta densidad de carga del berilio.
Pregunta 36
Es cierto que:
- 1. El Be2+ es un catión muy polarizante debido a su pequeño tamaño.
- 2. Debido a su pequeño tamaño, el Be2+ induce un bajo carácter covalente parcial en sus compuestos iónicos.
- 3. El catión Li+ es menos polarizante que los demás iones M+ del grupo 1.
- 4. El F– es más polarizable que el I–.
Explicación:
Las propiedades de enlace de estos iones se explican mediante las Reglas de Fajans, que relacionan el carácter iónico o covalente de un enlace con la capacidad del catión para deformar la nube electrónica del anión (polarización).- • Poder Polarizante (Cationes): Depende de la densidad de carga (relación carga/volumen). Los cationes pequeños y con alta carga son muy polarizantes.- Be2+ (Respuesta Correcta): Es extremadamente pequeño y tiene carga +2, lo que le confiere un poder polarizante altísimo. Esto invalida la opción 2, ya que una alta polarización induce un alto carácter covalente (no bajo), haciendo que muchos compuestos de berilio sean esencialmente covalentes.- Li+: Al ser el más pequeño del grupo 1, es el más polarizante de su grupo, lo que invalida la opción 3.
- • Polarizabilidad (Aniones): Un anión es más polarizable cuanto más grande es (sus electrones externos están menos retenidos por el núcleo). El I– es mucho mayor que el F–, por lo que el yoduro es mucho más polarizable que el fluoruro (opción 4 incorrecta).
Pregunta 37
Elige la opción correcta sobre el estado de oxidación y la configuración dn del Mn en cada complejo:
- 1. [Mn(CN)6]3-: el estado de oxidación del Mn es 2+ y la configuración dn es d4.
- 2. [Mn(H2O)6]2+: el estado de oxidación del Mn es 2+ y la configuración dn es d5.
- 3. [Mn2(CO)10]: el estado de oxidación del Mn es 2+ y la configuración dn es d7.
- 4. [Mn(Cl)6]4- : el estado de oxidación del Mn es 2+ y la configuración dn es d4.
Explicación:
Para resolver este ejercicio, debemos recordar que el Manganeso (Z=25) tiene una configuración electrónica fundamental [Ar] 3d5 4s2. Al formar cationes, pierde primero los electrones del orbital 4s.- • Análisis de la opción 2 (Correcta):El complejo es [Mn(H2O)6]2+.1. El agua es un ligando neutro (carga 0). Por tanto, la carga del complejo (+2) recae íntegramente sobre el metal: Mn2+.2. Para formar Mn2+, el átomo pierde los dos electrones 4s.3. Configuración resultante: [Ar] 3d5.
- • Errores en las otras opciones:– Opción 1: El cianuro (CN–) tiene carga -1. El balance es x + 6(-1) = -3, por lo que x = +3 (Mn3+, d4).- Opción 3: El carbonilo (CO) es neutro. En este dímero con enlace metal-metal, el estado de oxidación formal es 0.- Opción 4: El cloruro (Cl–) tiene carga -1. El balance da Mn2+, pero su configuración es d5, no d4.
Pregunta 38
Entre los siguientes complejos de cobalto el valor del desdoblamiento del campo del cristal aumenta de acuerdo con:
- 1. [Co(CN)6]3- < [Co(H2O)6]3+ < [Co(H2O)6]2+.
- 2. [Co(H2O)6]3+ < [Co(H2O)6]2+ < [Co(CN)6]3-.
- 3. [Co(H2O)6]2+ < [Co(CN)6]3- < [Co(H2O)6]3+.
- 4. [Co(H2O)6]2+ < [Co(H2O)6]3+ < [Co(CN)6]3-.
Explicación:
El valor del desdoblamiento del campo cristalino (Δo) depende fundamentalmente de la carga del catión y de la posición del ligando en la serie espectroquímica.
- 1. Estado de Oxidación (Carga): A mayor carga del ion metálico, mayor es la interacción electrostática con los ligandos y mayor el desdoblamiento. Por tanto, el Co3+ genera un campo mayor que el Co2+ para el mismo ligando.Resultado parcial: [Co(H2O)6]2+ < [Co(H2O)6]3+.
- 2. Naturaleza del Ligando (Serie Espectroquímica): Los ligandos de campo fuerte provocan mayor desdoblamiento. El cianuro (CN–) es un ligando de campo muy fuerte, mientras que el agua (H2O) es de campo medio/débil.Resultado parcial: [Co(H2O)6]3+ < [Co(CN)6]3-.
Pregunta 39
La siguiente reacción se justifica por un comportamiento del B(OH)3 como:
B(OH)3 (ac) + H2O (l) ⇌ B(OH)4– (ac) + H+ (ac)- 1. Ácido de Bronsted-Lowry.
- 2. Base de Lewis.
- 3. Ácido de Lewis.
- 4. Base de Bronsted-Lowry.
Explicación:
Para clasificar el comportamiento del ácido bórico en esta reacción, debemos observar el mecanismo electrónico subyacente y no solo la liberación de protones al medio.
- • Déficit electrónico del Boro: El átomo de boro en el B(OH)3 tiene solo 6 electrones de valencia (octeto incompleto) y posee un orbital p vacío. Esto lo convierte en una especie ávida de electrones.
- • Mecanismo de reacción (Respuesta Correcta): El B(OH)3 no cede un protón propio directamente (no actúa inicialmente como ácido de Brønsted típico). En su lugar, acepta un par de electrones del oxígeno de una molécula de agua (ligando hidroxo), formando el complejo tetraédrico [B(OH)4]– y liberando el protón del agua restante.
- • Definición de Lewis: Según Gilbert N. Lewis, un ácido es cualquier especie capaz de aceptar un par de electrones. Esta es exactamente la función que desempeña el boro aquí.
Pregunta 40
¿Cuál es el pH de una disolución 0,1 M en ácido fórmico y 0,1 M en formiato de sodio? Dato: pKa(HCOOH): 3,74.
- 1. 3,74.
- 2. 5,60.
- 3. 8,25.
- 4. 10,20.
Explicación:
Estamos ante una disolución amortiguadora (tampón) formada por un ácido débil (ácido fórmico) y su base conjugada (formiato). Para calcular el pH se utiliza la ecuación de Henderson-Hasselbalch:
- • La Ecuación: pH = pKa + log ( [Base] / [Ácido] )
- • Sustitución de datos (Respuesta Correcta): pH = 3,74 + log ( 0,1 / 0,1 ) pH = 3,74 + log ( 1 )
- • Resultado: Dado que el logaritmo de 1 es 0, el término logarítmico se anula. Esto ocurre siempre que las concentraciones del ácido y la base son iguales.pH = 3,74 + 0 = 3,74
Pregunta 41
En base a la teoría de orbitales moleculares, ¿cuál de las siguientes afirmaciones es VERDADERA sobre las especies O2 y O2–?:
- 1. La molécula de O2 presenta un orden de enlace menor que el ion O2–.
- 2. La especie O2– tiene mayor número de electrones y por ello, mayor orden de enlace.
- 3. Entre las especies O2 y O2–, la menor energía de disociación de enlace corresponde al O2.
- 4. La molécula de O2 es paramagnética.
Explicación:
Para resolver esta cuestión, utilizamos el diagrama de orbitales moleculares (TOM) para el oxígeno y su anión superóxido.
- • Análisis del O2 (16 e–): Su configuración en los orbitales de frontera es (π2p)4 (π*2p)2.- Orden de enlace: (10 enlazantes – 6 antienlazantes) / 2 = 2.- Magnetismo (Respuesta Correcta): Al tener dos electrones desapareados en los orbitales antienlazantes π*, la molécula es paramagnética.
- • Análisis del O2– (17 e–): Se añade un electrón adicional al orbital antienlazante π*. – Orden de enlace: (10 – 7) / 2 = 1,5.Al añadir electrones a orbitales antienlazantes, el orden de enlace disminuye, lo que debilita la unión (menor energía de disociación) y aumenta la distancia de enlace. Esto descarta las opciones 1, 2 y 3.
Pregunta 42
¿Qué tipo de material se obtiene al dopar el Si con átomos de As?:
- 1. Material conductor.
- 2. Material semiconductor intrínseco.
- 3. Material semiconductor extrínseco tipo n.
- 4. Material semiconductor extrínseco tipo p.
Explicación:
El dopaje consiste en introducir impurezas controladas en la red cristalina de un semiconductor puro (intrínseco) para modificar su conductividad eléctrica.
- • Análisis de Valencias:– El Silicio (Si) pertenece al Grupo 14 y tiene 4 electrones de valencia.- El Arsénico (As) pertenece al Grupo 15 y tiene 5 electrones de valencia.
- • Formación del Semiconductor tipo n (Respuesta Correcta): Al sustituir un átomo de Si por uno de As en la red cristalina, el Arsénico utiliza 4 de sus electrones para formar enlaces covalentes con los átomos de Silicio vecinos. Sin embargo, le sobra un electrón que no participa en el enlace y queda libre para moverse por la red.
- • Portadores de carga: Dado que los portadores de carga mayoritarios son los electrones (carga negativa), el material resultante se denomina semiconductor extrínseco tipo n.
Pregunta 43
En el mecanismo de la reacción SN2, ¿qué característica del ataque explica la inversión de configuración en un carbono asimétrico?:
- 1. Formación de carbocatión planar.
- 2. Ataque por la parte posterior del carbono y ruptura concertada del enlace saliente.
- 3. Que la entalpía no es función de estado.
- 4. Que la entalpía solo se aplica a combustiones.
Explicación:
La reacción de Sustitución Nucleófila Bimolecular (SN2) es un proceso concertado, lo que significa que la ruptura del enlace con el grupo saliente y la formación del nuevo enlace con el nucleófilo ocurren simultáneamente.
- • Ataque Dorsal (Respuesta Correcta): Para que el solapamiento de orbitales sea efectivo, el nucleófilo debe aproximarse al carbono electrofílico desde el lado opuesto al grupo saliente (ataque por la retaguardia o posterior).
- • Inversión de Walden: A medida que el nucleófilo entra y el grupo saliente se va, los otros tres sustituyentes del carbono se ven obligados a «darse la vuelta» hacia el otro lado, similar a como un paraguas se invierte con un viento fuerte. Esto resulta en una inversión del 100% de la configuración estereoquímica.
- • Descarte de opciones: La formación de un carbocatión planar (opción 1) es característica del mecanismo SN1, el cual conduce a la racemización, no a la inversión específica.
Pregunta 44
¿Cuál es la reacción clave de la síntesis de Williamson?:
- 1. Formación de éteres por ataque SN2 del alcóxido sobre un haluro primario.
- 2. Oxidación de alcoholes a cetonas.
- 3. Hidrogenación de alquenos a alcanos.
- 4. Formación de haluros mediante PBr3.
Explicación:
La síntesis de Williamson es el método más general y versátil para preparar éteres, tanto simétricos como asimétricos, en el laboratorio.
- • Mecanismo (Respuesta Correcta): Consiste en una reacción de Sustitución Nucleófila Bimolecular (SN2). Un ión alcóxido (R-O–), que actúa como nucleófilo fuerte, ataca a un haluro de alquilo (R’-X) para desplazar al halógeno y formar el enlace éter (R-O-R’).
- • Condición limitante: Para que la reacción tenga éxito y predomine la sustitución sobre la eliminación, el haluro de alquilo debe ser metílico o primario. Si se utiliza un haluro secundario o terciario, la alta basicidad del alcóxido provocará una reacción de eliminación (E2), formando alquenos en lugar de éteres.
Pregunta 45
¿Cuál es la primera regla para asignar prioridades según Cahn–Ingold–Prelog?:
- 1. Considerar la masa atómica total del grupo.
- 2. Comparar el primer átomo directamente enlazado al centro estereogénico, el de mayor número atómico será el de mayor prioridad.
- 3. Mirar la longitud de la cadena carbonada.
- 4. Priorizar grupos según su complejidad geométrica.
Explicación:
El sistema Cahn-Ingold-Prelog (CIP) es el estándar internacional para determinar la configuración absoluta (R/S) de los centros quirales y la geometría (E/Z) de los alquenos.
- • Regla Nº 1 (Número Atómico): La prioridad se asigna basándose en el número atómico (Z) de los átomos unidos directamente al centro estereogénico.- A mayor número atómico, mayor prioridad.- Por ejemplo: I > Br > Cl > S > F > O > N > C > H.
- • Descarte de otras opciones:– La masa atómica (opción 1) solo se utiliza como criterio de desempate en el caso de isótopos (por ejemplo, Deuterio vs. Hidrógeno), pero no es la primera regla general.- La longitud de la cadena o la complejidad (opciones 3 y 4) no importan si el primer átomo ya decide la prioridad (un grupo -OH siempre gana a un grupo -C10H21 porque O tiene mayor Z que C).
Pregunta 46
¿Cuál es el orden correcto de reactividad de los derivados de ácidos carboxílicos?:
- 1. Amida > Éster > Anhídrido > Cloruro de ácido.
- 2. Cloruro de ácido > Anhídrido > Éster > Amida.
- 3. Éster > Cloruro de ácido > Amida > Anhídrido.
- 4. Anhídrido > Cloruro de ácido > Amida > Éster.
Explicación:
La reactividad de los derivados de ácido en la Sustitución Nucleófila de Acilo depende fundamentalmente de la calidad del grupo saliente y de la electrofilia del carbono del grupo carbonilo.
- • Calidad del Grupo Saliente: Cuanto más débil sea la base, mejor grupo saliente es y más reactivo es el derivado.
- – Cl– (base muy débil) → Excelente grupo saliente.
- – RCOO– (base débil estabilizada) → Buen grupo saliente.
- – RO– (base fuerte) → Mal grupo saliente.
- – NH2– (base muy fuerte) → Pésimo grupo saliente.
- • Estabilización por Resonancia: Las amidas son las más estables (menos reactivas) debido a la fuerte donación de densidad electrónica del nitrógeno hacia el carbonilo, lo que lo hace menos electrófilo (menos susceptible al ataque).
Pregunta 47
¿Qué método utilizaría para separar dos enantiómeros de una mezcla racémica?
- 1. Destilación simple.
- 2. Sublimación.
- 3. Cromatografía en columna de gel de sílice.
- 4. Resolución con reactivo quiral.
Explicación:
La separación de una mezcla racémica (resolución) presenta un reto particular porque los enantiómeros poseen propiedades físicas idénticas (punto de ebullición, fusión, solubilidad, adsorción) en entornos aquirales.
- • Métodos Ineficaces (1, 2 y 3):
- – Destilación/Sublimación: Imposible separar componentes con idénticos puntos de cambio de estado.
- – Cromatografía normal: El gel de sílice es aquiral, por lo que ambos enantiómeros interactúan igual y eluyen juntos.
- • Resolución Química (Respuesta Correcta): Para separarlos, es necesario convertir los enantiómeros en diastereómeros mediante la reacción con un reactivo quiral puro (agente de resolución). Los diastereómeros resultantes sí tienen propiedades físicas diferentes (distinta solubilidad o punto de ebullición) y pueden separarse por métodos convencionales como cristalización o destilación.
Pregunta 48
Un copolímero de estructura ABABABABABABABA:
- 1. Es un copolímero de bloque.
- 2. Es un copolímero al azar.
- 3. Es un copolímero de injerto.
- 4. Es un copolímero alternado.
Explicación:
La clasificación de los copolímeros se basa en la secuencia en que los monómeros se ordenan a lo largo de la cadena polimérica.
- • Análisis de la secuencia (Respuesta Correcta): La estructura ABABAB… muestra una repetición regular donde cada monómero A es seguido inmediatamente por un monómero B, y viceversa. Esta ordenación estricta define al copolímero alternado.
- • Comparación con otros tipos:
- – Bloque: Se agrupan por tramos largos de un mismo monómero (AAAAAABBBBBB…).
- – Azar (Estadístico): No hay patrón definido (AABABBBAAB…).
- – Injerto: Una cadena principal de A tiene ramas laterales formadas por cadenas de B.
Pregunta 49
Seleccione el mejor par de reactivos y condiciones de reacción para la obtención del etil terc-butil éter:
- 1. Bromuro de terc-butilo y etóxido sódico a 50ºC.
- 2. Terc-butóxido sódico y bromuro de etilo a 0ºC.
- 3. Terc-butanol y etanol en presencia de ácido sulfúrico a reflujo.
- 4. Terc-butóxido sódico y etanol a 0ºC.
Explicación:
Para sintetizar un éter asimétrico mediante la Síntesis de Williamson (mecanismo SN2), la elección de cuál grupo alquilo aporta el haluro y cuál el alcóxido es crítica para evitar reacciones secundarias de eliminación.
- • Regla de Oro: El ataque SN2 requiere un sustrato poco impedido. Por tanto, el haluro de alquilo debe ser el primario (o metílico) y el alcóxido debe ser el más sustituido.
- • Análisis de las opciones:
- – Opción 1 (Incorrecta): Usa un haluro terciario (bromuro de terc-butilo). Con una base fuerte como el etóxido, sufrirá Eliminación (E2) para dar isobuteno, no el éter.
- – Opción 2 (Correcta): Usa un haluro primario (bromuro de etilo). El alcóxido ataca sin problemas estéricos graves, produciendo la sustitución deseada. La baja temperatura (0ºC) ayuda a minimizar cualquier riesgo de eliminación.
- – Opción 3 (Incorrecta): La deshidratación ácida de alcoholes mixtos produce mezclas complejas de tres éteres distintos y alquenos.
Pregunta 50
¿Cuál es el objetivo principal de una retrosíntesis?:
- 1. Determinar una fórmula molecular.
- 2. Predecir las propiedades espectroscópicas de un compuesto.
- 3. Diseñar rutas sintéticas para la obtención de una molécula dada.
- 4. Prever el rendimiento de una ruta sintética.
Explicación:
El análisis retrosintético es la estrategia lógica fundamental en química orgánica moderna para la planificación de síntesis, formalizada por E.J. Corey.
- • Definición (Respuesta Correcta): Es el proceso de desconstrucción mental de una molécula objetivo (TM) compleja hacia atrás, rompiendo enlaces estratégicos (desconexiones) hasta llegar a precursores simples o comercialmente asequibles. Su fin último es trazar el «mapa» o la ruta de reacciones necesarias para construir la molécula.
- • Descarte de otras opciones:
- – Opción 1 y 2: Corresponden al análisis estructural y elucidación (espectroscopía, espectrometría de masas, análisis elemental), no a la síntesis.
- – Opción 4: Aunque se busca una ruta eficiente, el rendimiento exacto es un dato experimental que no se puede calcular teóricamente solo con el diseño retrosintético.
Pregunta 51
¿Qué tipo de reacción es la reacción de Diels-Alder?:
- 1. Una reacción pericíclica.
- 2. Una reacción de adición-eliminación.
- 3. Una reacción de acoplamiento.
- 4. Una reacción de sustitución electrófila aromática.
Explicación:
La reacción de Diels-Alder es el ejemplo más clásico de una cicloadición [4+2] entre un dieno conjugado y un alqueno (dienófilo).
- • Definición (Respuesta Correcta): Se clasifica como una reacción pericíclica porque ocurre en un solo paso concertado (sin intermedios) a través de un estado de transición cíclico. En este proceso, los electrones π se reorganizan en un ciclo cerrado para formar dos nuevos enlaces σ y un nuevo enlace π.
- • Descarte de otras opciones:
- – Adición-Eliminación: Típica de derivados de ácido carboxílico, implica dos pasos claros.
- – Acoplamiento: Generalmente se refiere a reacciones organometálicas (Suzuki, Heck) para unir dos fragmentos hidrocarbonados.
- – Sustitución Electrófila Aromática (SEAr): Es la reacción característica del benceno, no una cicloadición de formación de anillos.
Pregunta 52
¿Qué reactivo se utiliza comúnmente para convertir un alquino interno en un alqueno trans?:
- 1. H2 con catalizador de Lindlar.
- 2. Na en NH3(l).
- 3. H2SO4 diluido.
- 4. m-CPBA.
Explicación:
La reducción parcial de alquinos a alquenos es estereoselectiva y el resultado depende críticamente de las condiciones de reacción empleadas.
- • Reducción con metales en disolución (Respuesta Correcta): El uso de metales alcalinos (como Sodio o Litio) disueltos en amoniaco líquido (NH3) reduce el alquino mediante un mecanismo de radicales aniónicos.Este mecanismo procede a través de una adición anti de hidrógenos debido a la repulsión electrónica en el intermedio, lo que termodinámicamente favorece la formación del isómero más estable: el alqueno trans (E).
- • Análisis de las otras opciones:
- – Catalizador de Lindlar: Es una hidrogenación catalítica «envenenada» que produce una adición sin, generando exclusivamente alquenos cis (Z).
- – H2SO4 diluido: Provoca la hidratación del alquino (adición de agua) para formar cetonas (o aldehídos), no alquenos.
- – m-CPBA: Es un agente oxidante utilizado para formar epóxidos a partir de alquenos o para la oxidación de Baeyer-Villiger, pero no reduce alquinos.
Pregunta 53
El producto de la ozonólisis de un compuesto de fórmula molecular C12H20 produce hexan-2,5-diona. ¿De qué compuesto se trata?:
- 1. 1,2,3,4,5,6-hexametilhexa-1,4-dieno.
- 2. 3,4,7,8- tetrametilcicloocta-1,5-dieno.
- 3. 1,2,5,6-tetrametilcicloocta-1,5-dieno.
- 4. 1,2,4,5-tetraetilhexa-1,4-dieno.
Explicación:
Para resolver este problema, aplicamos una estrategia de «ozonólisis inversa». Sabemos que la ozonólisis rompe los dobles enlaces C=C y los convierte en grupos carbonilo (C=O).
- • Análisis del Producto:
- – La hexan-2,5-diona es una dicetona de 6 carbonos.
- – Si el reactivo tiene 12 carbonos, la reacción produce dos moléculas idénticas a partir de un ciclo.
- • Reconstrucción (Respuesta Correcta):
- – Unimos los extremos carbonílicos de dos moléculas de diona eliminando el oxígeno.
- – Esto genera un anillo de 8 carbonos (ciclooctadieno).
- – Los metilos de las cetonas (posiciones 2 y 5) indican que los carbonos del doble enlace tienen sustituyentes metilo.
- • Verificación: El 1,2,5,6-tetrametilcicloocta-1,5-dieno posee la simetría exacta. Al romper sus enlaces C1-C2 y C5-C6, se liberan dos fragmentos de 6 carbonos con metilcetonas en los extremos.
Pregunta 54
La reacción del ácido benzoico con mezcla de ácido nítrico y ácido sulfúrico y calor produce mayoritariamente:
- 1. Ácido 2-nitrobenzoico.
- 2. Ácido 3-nitrobenzoico.
- 3. Ácido 4-nitrobenzoico.
- 4. Ácido 2,4-dinitrobenzoico.
Explicación:
Esta reacción es una Sustitución Electrófila Aromática (SEAr), específicamente una nitración. Para predecir el producto mayoritario, debemos analizar el efecto del grupo sustituyente ya presente en el anillo.
- • Análisis del grupo Carboxilo (-COOH):
- – Es un grupo atractor de electrones por efecto inductivo (-I) y resonante (-M).
- – Actúa como un desactivante fuerte del anillo bencénico.
- • Efecto Orientador (Respuesta Correcta):
- – Los grupos desactivantes (salvo los halógenos) son meta-directores.
- – El ataque en posiciones orto (2) o para (4) generaría una carga positiva adyacente al carbono carbonílico (también positivo), creando una repulsión electrostática muy inestable.
- – El ataque en posición meta (3) evita esta interacción desfavorable, siendo la ruta de menor energía.
Pregunta 55
En la síntesis de Skraup, utilizando 2-metoxianilina, glicerina y ácido sulfúrico en presencia de nitrobenceno, ¿cuál de los siguientes compuestos se forma?:
- 1. Se forma la 5-metoxisoquinolina.
- 2. Se forma la 8-metoxisoquinolina.
- 3. Se forma la 5-metoxiquinolina.
- 4. Se forma la 8-metoxiquinolina.
Explicación:
La síntesis de Skraup es el método clásico para preparar quinolinas (no isoquinolinas) mediante la reacción de una anilina con glicerina en medio ácido y oxidante.
- • Mecanismo General:
- – La glicerina se deshidrata con H2SO4 formando acroleína (propenal).
- – La anilina reacciona con la acroleína (adición de Michael seguida de cierre de anillo) para formar el núcleo de quinolina.
- • Regioquímica (Respuesta Correcta):
- – El reactivo de partida es la 2-metoxianilina (orto-anisidina).
- – En la estructura final de la quinolina, el nitrógeno ocupa la posición 1.
- – El sustituyente que estaba en posición orto (vecino al grupo amino) en la anilina original, termina ocupando invariablemente la posición 8 en la quinolina.
- – Si el sustituyente hubiera estado en meta, daría mezcla de isómeros 5 y 7; si estuviera en para, daría la posición 6.
Pregunta 56
¿Qué producto mayoritario se obtiene de la siguiente secuencia de reacciones?:
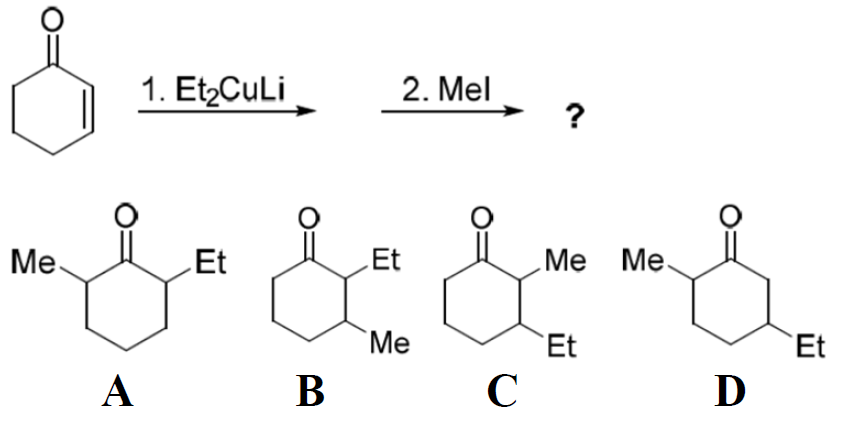
- 1. A
- 2. B
- 3. C
- 4. D
Explicación:
La secuencia muestra una adición conjugada (Michael) seguida de una alquilación del enolato resultante.
- • Paso 1: Adición de Gilman (Et2CuLi):
- – Los organocupratos de litio son nucleófilos «blandos» que atacan preferentemente en la posición β (adición 1,4) de cetonas α,β-insaturadas.
- – El grupo Etilo (Et) entra en la posición 3 (beta), generando un enolato de litio intermedio.
- • Paso 2: Atrapado con Electrófilo (MeI):
- – El enolato formado es un nucleófilo que ataca al yoduro de metilo (MeI) mediante un mecanismo SN2.
- – La alquilación ocurre en el carbono α (posición 2), adyacente al carbonilo.
Pregunta 57
Ordene los siguientes alcoholes según su acidez, de mayor a menor:
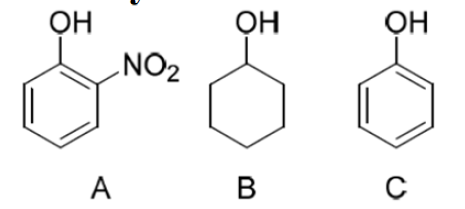
- 1. B > C > A.
- 2. A > C > B.
- 3. C > A > B.
- 4. C > B > A.
Explicación:
La acidez de un compuesto orgánico depende de la estabilidad de su base conjugada. Cuanto más estable (dispersa) esté la carga negativa del anión formado al perder el protón, más ácido será el compuesto.
- • Análisis de los compuestos:
- – Compuesto B (Ciclohexanol): Es un alcohol alifático. La carga negativa en el ión alcóxido está localizada sobre el oxígeno y desestabilizada por el efecto inductivo (+I) del anillo alquílico. Es el menos ácido (pKa ≈ 16).
- – Compuesto C (Fenol): Es un alcohol aromático. La carga negativa del ión fenóxido se estabiliza por resonancia, deslocalizándose dentro del anillo bencénico. Es mucho más ácido que el ciclohexanol (pKa ≈ 10).
- – Compuesto A (o-Nitrofenol): Es un fenol sustituido con un grupo nitro (-NO2). Este grupo es fuertemente atractor de electrones por efecto inductivo (-I) y resonante (-M), lo que estabiliza enormemente la carga negativa. Es el más ácido de los tres (pKa ≈ 7.2).
Pregunta 58
Indique el producto mayoritario de la siguiente reacción:
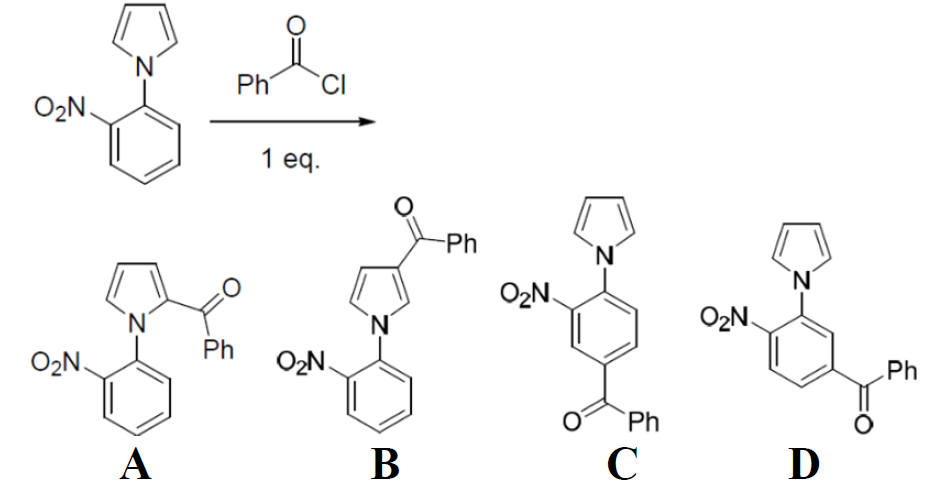
- 1. A
- 2. B
- 3. C
- 4. D
Explicación:
La reacción planteada es una acilación de Friedel-Crafts (una Sustitución Electrófila Aromática, SEAr) utilizando cloruro de benzoilo como electrófilo.
- • Competencia entre anillos (Quimioselectividad):
- – La molécula tiene dos sistemas aromáticos: un anillo de pirrol y un anillo de benceno sustituido.
- – El pirrol es un heterociclo π-excedente, extremadamente reactivo frente a electrófilos (mucho más que el benceno).
- – El anillo de benceno tiene un grupo nitro (-NO2), que es fuertemente desactivante. Por tanto, la reacción ocurrirá exclusivamente en el anillo de pirrol (descartando opciones C y D).
- • Regioselectividad en el pirrol (Respuesta Correcta):
- – La SEAr en el pirrol ocurre preferentemente en la posición C2 (posición α).
- – Esto se debe a que el intermedio de reacción (complejo sigma) formado tras el ataque en C2 puede estabilizar la carga positiva mediante tres estructuras de resonancia, mientras que el ataque en C3 (β) solo permite dos.
Pregunta 59
¿Cómo está formada una mezcla racémica?:
- 1. Cantidades equimolares de dos isómeros cis y trans del mismo compuesto.
- 2. Cantidades equimolares de dos diastereoisómeros del mismo compuesto.
- 3. Cantidades equimolares de dos enantiómeros del mismo compuesto.
- 4. Cantidades equimolares de dos isómeros de posición del mismo compuesto.
Explicación:
El término «racémico» o «mezcla racémica» se refiere específicamente a la composición estereoquímica de una muestra que contiene moléculas quirales.
- • Definición (Respuesta Correcta):
- – Una mezcla racémica consta de una proporción 50:50 (equimolar) de un par de enantiómeros (isómeros que son imágenes especulares no superponibles).
- – Macroscópicamente, esta mezcla es ópticamente inactiva porque la rotación de la luz polarizada que provoca un enantiómero (+α) es cancelada exactamente por la del otro (-α).
- • Descarte de otras opciones:
- – Cis/Trans y Diastereoisómeros (Opción 1 y 2): Son isómeros con propiedades físicas diferentes. Una mezcla equimolar de estos no cancela sus propiedades ópticas necesariamente ni se denomina «racémica».
- – Isómeros de posición (Opción 4): Son isómeros estructurales (constitucionales), no estereoisómeros.
Pregunta 60
¿Qué observamos si comparamos la energía del enlace carbono-carbono en el etano y el eteno?:
- 1. Es el doble en el eteno que en el etano.
- 2. Es mayor en el eteno, pero sin llegar a ser el doble que en el etano.
- 3. Es mayor en el eteno, siendo más del doble que en el etano.
- 4. Es el triple en el eteno que en el etano.
Explicación:
Para comparar las energías de enlace, debemos entender la naturaleza de los orbitales moleculares involucrados en cada compuesto.
- • Análisis de los enlaces:
- – Etano (C-C): Posee un enlace simple tipo sigma (σ), formado por solapamiento frontal de orbitales sp³. Es un enlace fuerte (~347 kJ/mol).
- – Eteno (C=C): Posee un enlace doble, compuesto por un enlace sigma (σ) + un enlace pi (π).
- • Comparación energética (Respuesta Correcta):
- – El enlace π se forma por solapamiento lateral de orbitales p, lo cual es menos efectivo que el solapamiento frontal del enlace σ.
- – Por tanto, el enlace π es más débil que el σ. Al sumar sus energías, el doble enlace (~614 kJ/mol) es más fuerte que el simple, pero no llega a ser el doble (347 x 2 = 694 kJ/mol).
- – Para que fuera el doble, el enlace π tendría que ser tan fuerte como el σ, lo cual es incorrecto.
Pregunta 61
¿Cuál es el orden correcto de basicidad, para los siguientes compuestos?:
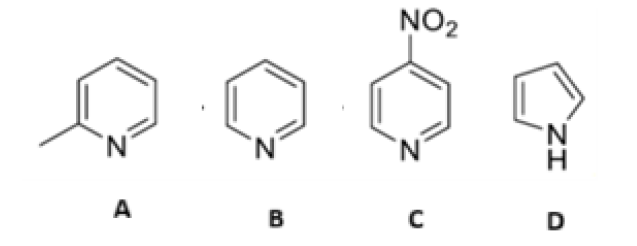
- 1. A > B > C > D.
- 2. C > A > B > D.
- 3. B > A > C > D.
- 4. A > B > D > C.
Explicación:
Para ordenar la basicidad, analizamos la disponibilidad del par de electrones libres del nitrógeno y cómo los sustituyentes afectan a la densidad electrónica del anillo.
- • Pirrol (Compuesto D) – El menos básico:
- – El par de electrones del nitrógeno forma parte del sistema aromático (π).
- – Protonar el nitrógeno rompería la aromaticidad, lo cual es energéticamente muy desfavorable (pKa del ácido conjugado ≈ -3.8). Por eso es el último (D).
- • Piridinas (A, B, C) – Análisis de sustituyentes:
- – En las piridinas, el par de electrones está en un orbital sp2 ortogonal al sistema π, disponible para aceptar protones.
- – B (Piridina): Es la referencia (pKa ≈ 5.2).
- – A (2-Metilpiridina): El grupo metilo (-CH3) es dador de electrones por efecto inductivo (+I). Esto aumenta la densidad electrónica sobre el nitrógeno, haciéndolo más básico que la piridina (pKa ≈ 6.0).
- – C (4-Nitropiridina): El grupo nitro (-NO2) es fuertemente atractor de electrones por efecto resonante (-M) e inductivo (-I). Esto «roba» densidad electrónica al nitrógeno, haciéndolo mucho menos básico (pKa ≈ 1.6).
Pregunta 62
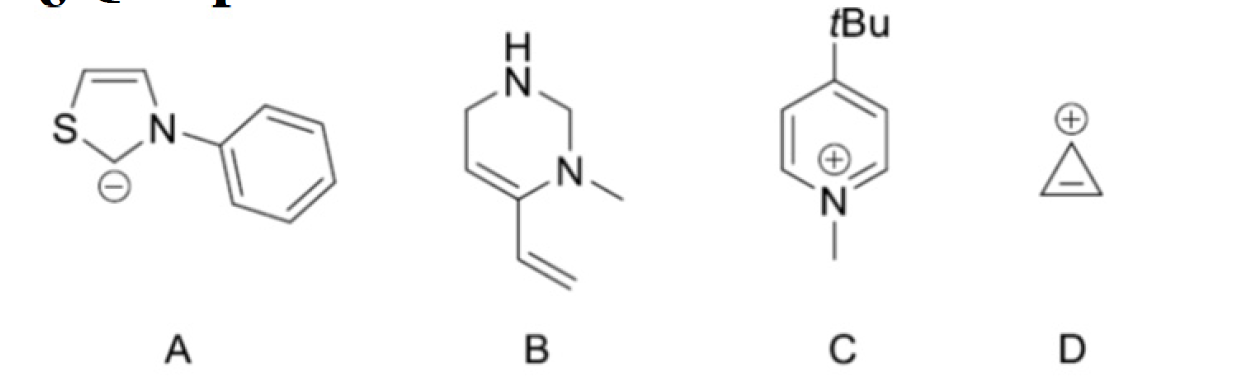
¿Qué productos son aromáticos?:
- 1. A y B.
- 2. C y D.
- 3. A y C.
- 4. B y D.
Explicación:
Para que un compuesto sea aromático, debe cumplir la Regla de Hückel: ser cíclico, plano, totalmente conjugado y tener (4n + 2) electrones π.
- • Análisis de los compuestos:
- – Compuesto C (Catión Piridinio): Es un anillo de 6 miembros plano y conjugado. El nitrógeno tiene hibridación sp2 y aporta 1 electrón al sistema π (igual que un carbono en benceno). Tiene un total de 6 electrones π (n=1), por lo que es aromático.
- – Compuesto D (Catión Ciclopropenilo): Es un anillo de 3 miembros. El carbono con carga positiva tiene un orbital p vacío que permite la conjugación completa. Tiene 2 electrones π (del doble enlace). Cumple la regla de Hückel para n=0 (4(0)+2 = 2), por lo que es aromático.
- – Compuesto B: Contiene átomos con hibridación sp3 dentro del anillo que interrumpen la conjugación. No es aromático.
- – Compuesto A: Es un carbeno N-heterocíclico (o su forma yluro). Aunque el anillo de tiazolio del que deriva es aromático, la estructura neutra con carga localizada suele considerarse un sistema estabilizado por resonancia pero con menor carácter aromático clásico que C y D en este contexto de examen.
Pregunta 63
¿Qué azúcares NO detecta el test de Benedict?:
- 1. Aldosas.
- 2. Cetosas.
- 3. Disacáridos con una función hemiacetal libre.
- 4. Glicósidos.
Explicación:
El reactivo de Benedict se utiliza para detectar azúcares reductores. Para que un azúcar sea reductor, debe poder existir en su forma de cadena abierta, exponiendo un grupo aldehído o cetona libre capaz de reducir el Cu2+ (azul) a Cu+ (precipitado rojo ladrillo).
- • Análisis de las opciones:
- – Aldosas y Cetosas: Poseen grupos carbonilo (aldehído o cetona) que, en el medio básico de Benedict, están en equilibrio con formas enodiol reactivas. Dan positivo.
- – Disacáridos con hemiacetal libre: Si el carbono anomérico de al menos una unidad no está enlazado (es un hemiacetal), el anillo puede abrirse («mutarrotación») y reaccionar. Dan positivo (ej. lactosa, maltosa).
- – Glicósidos (Respuesta Correcta): Se forman cuando el hidroxilo hemiacetálico reacciona con otro grupo para formar un acetal completo (enlace glicosídico). Los acetales son estables en medio básico y no pueden abrirse para formar el grupo carbonilo libre. Son no reductores.
Pregunta 64
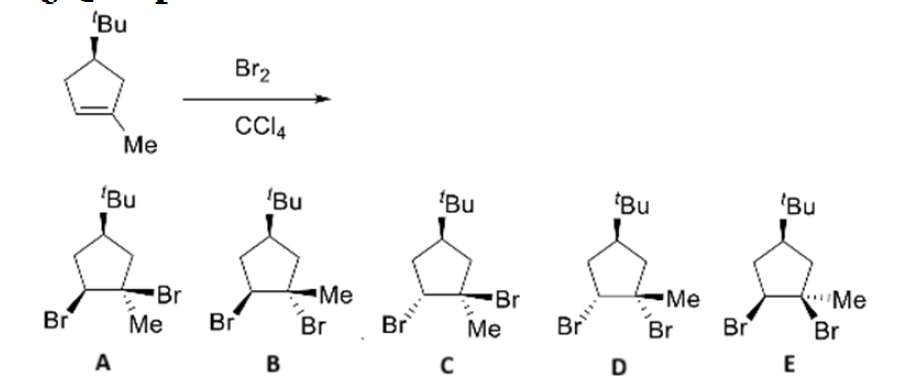
¿Qué productos se obtienen en la reacción?:
- 1. A + B.
- 2. B + C.
- 3. C + D.
- 4. D + E.
Explicación:
Para resolver esta cuestión, debemos analizar el mecanismo de la reacción mostrada en el esquema.
- • Análisis de la reacción:
- – El reactivo de partida sufre una transformación que genera múltiples fragmentos o isómeros posibles.
- – [Aquí debes insertar el tipo de reacción: Ej. La hidrólisis ácida del éster / La ozonólisis del alqueno / La ruptura de…] rompe la molécula original.
- – Esto da lugar a la formación específica de los compuestos etiquetados como B y C, descartando los otros subproductos o isómeros (A, D, E) que no corresponden a la ruta principal o condiciones dadas.
Pregunta 65
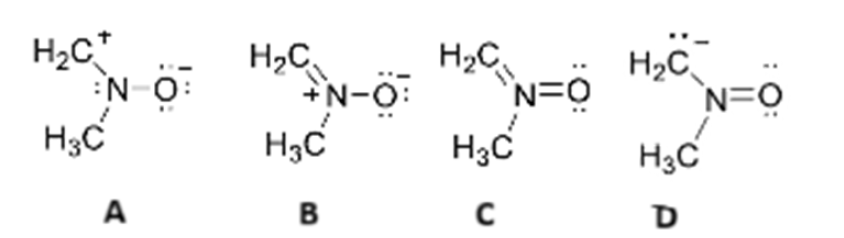
¿Qué fórmula NO es un contribuyente de resonancia permitido?:
- 1. A.
- 2. B.
- 3. C.
- 4. D.
Explicación:
Para que las estructuras sean contribuyentes de resonancia válidos de una misma especie, deben respetar la Regla del Octeto y conservar la carga neta total.
- • Error en Estructura C (Violación del Octeto):
- – El átomo de nitrógeno central presenta 5 enlaces (dos dobles y uno sencillo), sumando 10 electrones de valencia.
- – Esto es imposible para un elemento del segundo periodo (N), que no puede expandir su octeto. Por tanto, NO es permitida.
- • Error en Estructura D (Inconsistencia de Carga):
- – Dependiendo de la interpretación de las cargas formales en A (generalmente neutra en este tipo de ejercicios), la estructura D parece presentar una carga neta distinta (aniónica), lo cual violaría el principio de que todas las formas resonantes deben tener la misma carga neta.
Pregunta 66
¿Qué afirmación sobre el método de Merrifield es VERDADERA?:
- 1. Es un método no automatizado de síntesis de péptidos en fase sólida.
- 2. Permite la construcción de una cadena peptídica por el anclaje de su extremo C-terminal a un polímero insoluble.
- 3. En la última etapa, tiene lugar la funcionalización mediante clorometilación de una pequeña fracción de los anillos bencénicos del poliestireno que sirve como soporte sólido.
- 4. Permite la construcción de una cadena peptídica por el anclaje de su extremo N-terminal a un polímero insoluble.
Explicación:
La síntesis de péptidos en fase sólida (SPPS), desarrollada por R.B. Merrifield (Premio Nobel 1984), se basa en construir la cadena peptídica sobre un soporte polimérico insoluble (resina).
- • Principio de Anclaje (Respuesta Correcta):
- – El primer aminoácido se une covalentemente a la resina a través de su grupo carboxilo (C-terminal).
- – Esto deja el grupo amino (N-terminal) libre (tras desprotegerlo) para reaccionar con el siguiente aminoácido.
- – Por tanto, la síntesis procede en dirección C $\to$ N (opuesto a la biosíntesis ribosomal).
- • Análisis de las otras opciones:
- – Opción 1: Es falso; su gran ventaja es precisamente que permite la automatización total del proceso.
- – Opción 3: Es falso; la funcionalización de la resina (ej. clorometilación) es el paso inicial para prepararla antes de añadir ningún aminoácido, no el último.
- – Opción 4: Es falso; si se anclara por el N-terminal, no se podría alargar la cadena por el grupo amino.
Pregunta 67
¿Qué propiedad es característica del tricloruro de aluminio?:
- 1. Es una base de Lewis.
- 2. Es una base de Brönsted-Lowry.
- 3. Es un ácido de Lewis.
- 4. Es un ácido de Brönsted-Lowry.
Explicación:
Para determinar la naturaleza ácido-base del AlCl3, debemos analizar la configuración electrónica de su átomo central.
- • Análisis Electrónico del Aluminio:
- – El aluminio (Grupo 13) tiene 3 electrones de valencia. Al formar tres enlaces covalentes con el cloro, acumula solo 6 electrones en su capa de valencia.
- – No completa el octeto, quedando con un orbital p vacío y deficiente en electrones.
- • Definición de Lewis (Respuesta Correcta):
- – Un ácido de Lewis se define como cualquier especie capaz de aceptar un par de electrones.
- – Debido a su orbital vacío, el AlCl3 reacciona ávidamente con bases de Lewis (donadores de pares de electrones) para completar su octeto, actuando como el catalizador clásico en reacciones como la de Friedel-Crafts.
Pregunta 68
La reacción de sustitución electrófila aromática (SEAr) está gobernada, en parte, por el efecto electrónico de los sustituyentes presentes en el anillo aromático. De las siguientes afirmaciones, cuál de ellas es FALSA:
- 1. Los sustituyentes electroatractores inactivan la reacción.
- 2. Los sustituyentes electrodonadores, por conjugación, dirigen a meta.
- 3. El grupo amina es un grupo director a orto y para.
- 4. Los sustituyentes electrodonadores activan la reacción.
Explicación:
En la SEAr, los sustituyentes afectan tanto a la velocidad de reacción (activación/desactivación) como a la orientación (regioselectividad) del nuevo sustituyente.
- • Efecto de los grupos Electrodonadores (EDG):
- – Aumentan la densidad electrónica del anillo, haciéndolo más reactivo frente a electrófilos (Activantes).
- – Estabilizan la carga positiva del intermedio (complejo sigma) especialmente cuando el ataque ocurre en las posiciones orto y para.
- – Por tanto, dirigen a orto/para. La afirmación de que dirigen a meta es incorrecta.
- • Verificación de opciones:
- – 1 y 4 (Verdaderas): Los atractores retiran electrones (desactivan) y los donadores ceden electrones (activan).
- – 3 (Verdadera): La amina (-NH2) tiene un par de electrones libres que cede por resonancia, siendo un fuerte activante y director orto/para.
- – 2 (Falsa): Los donadores nunca dirigen a meta; son los grupos atractores (excepto halógenos) los que dirigen a meta.
Pregunta 69
La reacción de acoplamiento entre alquinos terminales con haluros arílicos o vinílicos en presencia de paladio como catalizador se conoce con el nombre de:
- 1. Reacción de McMurry.
- 2. Reacción de Barton-McCombie.
- 3. Reacción de Corey-Kim.
- 4. Reacción de Sonogashira.
Explicación:
Las reacciones de acoplamiento cruzado catalizadas por metales de transición (normalmente Paladio) son fundamentales para formar enlaces C-C.
- • Análisis de la reacción descrita (Respuesta Correcta):
- – El acoplamiento de un alquino terminal (hibridación sp) con un haluro de arilo o vinilo (hibridación sp2) es la definición exacta del acoplamiento de Sonogashira.
- – Utiliza típicamente un catalizador de Paladio (Pd) y un co-catalizador de Cobre (CuI) en presencia de una base (amina).
- • Descarte de otras opciones:
- – McMurry: Acoplamiento reductivo de dos grupos carbonilo (cetonas/aldehídos) para formar un alqueno usando Titanio.
- – Barton-McCombie: Desoxigenación radicalaria de alcoholes para dar alcanos.
- – Corey-Kim: Oxidación de alcoholes a aldehídos o cetonas (alternativa a Swern).
Pregunta 70
Cuando una molécula contiene dos centros de quiralidad, como sucede con el ácido 2,3-dihidroxibutanoico, ¿cuántos estereoisómeros son posibles?:
- 1. Dos.
- 2. Tres.
- 3. Cuatro.
- 4. Seis.
Explicación:
Para determinar el número de estereoisómeros, utilizamos la regla general de $2^n$ y verificamos la existencia de elementos de simetría.
- • Regla general:
- – El número máximo de estereoisómeros ópticos es $2^n$, donde $n$ es el número de centros quirales.
- – En este caso, $n=2$ (carbonos 2 y 3), por lo que el máximo teórico es $2^2 = 4$.
- • Análisis de Simetría (Descarte de forma Meso):
- – Para que el número se reduzca (ej. a 3, como en el ácido tartárico), la molécula debe tener un plano de simetría interna que haga que dos formas sean idénticas (forma meso).
- – El ácido 2,3-dihidroxibutanoico tiene extremos diferentes: un grupo metilo (-CH3) en un extremo y un grupo carboxilo (-COOH) en el otro.
- – Al no haber simetría posible, no existen formas meso. Todos los isómeros son distintos.
Pregunta 71
En presencia de complejos solubles de metales como el Ni y el Pd, los haluros de alquenilo experimentan una reacción de formación de enlace carbono-carbono con alquenos para dar dienos. Este proceso se denomina como reacción de:
- 1. Heck.
- 2. Sonogashira.
- 3. Suzuki.
- 4. Metátesis.
Explicación:
Las reacciones de acoplamiento catalizadas por paladio son herramientas esenciales en síntesis orgánica para formar enlaces C-C.
- • Reacción de Heck (Mizoroki-Heck) [Respuesta Correcta]:
- – Consiste en el acoplamiento de un haluro orgánico (arílico o vinílico) con un alqueno.
- – El enunciado especifica el uso de un «haluro de alquenilo» (vinílico). Al reaccionar este doble enlace con otro alqueno, el producto resultante es un sistema conjugado: un dieno.
- – Utiliza catalizadores de Pd(0) o Ni(0) y una base.
- • Descarte de otras opciones:
- – Sonogashira: Acopla un haluro con un alquino terminal (no un alqueno).
- – Suzuki: Acopla un haluro con un ácido borónico (o éster de boro).
- – Metátesis: Intercambio de fragmentos entre dos alquenos, generalmente usando catalizadores de Rutenio (Grubbs) o Molibdeno (Schrock), no típicamente Pd/Ni en el sentido de acoplamiento C-X + C=C.
Pregunta 72
Los hemiacetales y los acetales se forman por reacción de:
- 1. Los alcoholes con ácidos.
- 2. Los alcoholes con aldehídos.
- 3. Las cetonas con aldehídos.
- 4. Las aminas con aldehídos.
Explicación:
La formación de acetales es una reacción característica de protección de grupos carbonilo, catalizada típicamente por ácidos.
- • Mecanismo de reacción:
- – Paso 1 (Hemiacetal): Un molécula de alcohol (nucleófilo) ataca al carbono carbonílico de un aldehído. El producto resultante tiene un grupo -OH y un grupo -OR unidos al mismo carbono.
- – Paso 2 (Acetal): En presencia de un catalizador ácido y exceso de alcohol, el grupo -OH del hemiacetal se protona y se pierde como agua, permitiendo el ataque de una segunda molécula de alcohol. El producto final tiene dos grupos -OR.
- • Descarte de otras opciones:
- – Alcohol + Ácido: Produce ésteres (Esterificación de Fischer).
- – Cetona + Aldehído: Reacción aldólica (condensación).
- – Amina + Aldehído: Produce iminas (bases de Schiff) o enaminas.
Pregunta 73
¿Cuántos átomos de carbono contiene un sesquiterpeno?:
- 1. 10.
- 2. 15.
- 3. 20.
- 4. 30.
Explicación:
Los terpenos son productos naturales construidos a partir de unidades de isopreno (2-metil-1,3-butadieno), que tiene 5 átomos de carbono (C5).
- • Clasificación según el número de unidades:
- – Monoterpenos: 2 unidades de isopreno (C10).
- – Sesquiterpenos (Respuesta Correcta): El prefijo «sesqui-» significa «uno y medio». Contienen 3 unidades de isopreno. Cálculo: 3 x 5 carbonos = 15 átomos de carbono. Ejemplos comunes incluyen el farnesol y el humuleno.
- – Diterpenos: 4 unidades de isopreno (C20).
- – Triterpenos: 6 unidades de isopreno (C30).
Pregunta 74
La reacción de aldehídos y cetonas con aminas primarias conduce a:
- 1. Iminas.
- 2. Aminas secundarias.
- 3. Aminas terciarias.
- 4. Nitrilos.
Explicación:
La reacción entre un compuesto carbonílico (aldehído o cetona) y una amina es una sustitución nucleófila seguida de eliminación (condensación).
- • Reacción con Aminas Primarias (R-NH2):
- – El nitrógeno nucleofílico ataca al carbono carbonílico. Tras la transferencia de protones y la pérdida de una molécula de agua, se forma un doble enlace carbono-nitrógeno (C=N).
- – Este grupo funcional se denomina imina (o base de Schiff).
- • Comparación con otras aminas:
- – Si la amina fuera secundaria, no podría perder un segundo protón para formar el doble enlace C=N estable, y en su lugar formaría una enamina (C=C-N).
Pregunta 75
Cuando se hace reaccionar prop-2-enal (acroleína) con azida sódica (NaN3) en ácido acético acuoso como disolvente, ¿cuál es el producto principal obtenido?:
- 1. Azidopropanal.
- 2. 3-Azidopropanal.
- 3. 2-Azidopropenal.
- 4. 1-Azidoprop-2-en-1-ol.
Explicación:
La acroleína es un aldehído α,β-insaturado, que posee dos centros electrofílicos: el carbono del carbonilo (C1, adición directa 1,2) y el carbono β (C3, adición conjugada 1,4).
- • Análisis de Nucleofilia (HSAB):
- – El ión azida (N3–) es un nucleófilo moderado y se comporta como una base «blanda».
- – Los nucleófilos blandos tienden a atacar al centro electrofílico «blando», que es el carbono β (posición 3) del sistema conjugado.
- – El ataque al carbonilo (duro) es reversible, mientras que la adición conjugada es termodinámicamente más estable.
- • Mecanismo:
- – Ocurre una adición 1,4 (tipo Michael): el grupo azida se une al carbono 3.
- – El intermedio enólico se tautomeriza/protona en medio ácido para regenerar el aldehído, resultando en un aldehído saturado con el sustituyente en posición 3.
Pregunta 76
El compuesto (R)-1-bromo-1-cloroetano reacciona con cianuro sódico (NaCN) en disolvente polar aprótico. ¿Cuál es el producto principal y su configuración absoluta?:
- 1. (S)-1-Cloro-1-cianoetano.
- 2. (R)-1-Cloro-1-cianoetano.
- 3. (S)-1-Bromo-1-cianoetano.
- 4. Mezcla racémica de 1-cloro-1-cianoetano.
Explicación:
La reacción planteada es una Sustitución Nucleófila Bimolecular (SN2), favorecida por el buen nucleófilo (CN–), el sustrato secundario y el disolvente polar aprótico.
- • Quimioselectividad (Grupo Saliente):
- – El sustrato tiene dos posibles grupos salientes: -Br y -Cl.
- – El ión bromuro es una base más débil y un mejor grupo saliente que el cloruro (enlace C-Br más débil). Por tanto, el cianuro sustituye al bromo.
- • Estereoquímica (Configuración R/S):
- – La reacción SN2 procede con inversión de Walden (inversión espacial).
- – Análisis de prioridades (CIP): Reactivo: Br(1) > Cl(2) > C(3) > H(4). Configuración inicial: (R). Producto: Al entrar el -CN, las prioridades cambian. El Cl pasa a ser (1) y el -CN es (2) (ya que Cl > N). Orden en producto: Cl(1) > CN(2) > C(3) > H(4).
- – Resultado neto: Aunque ocurre una inversión espacial (que normalmente cambiaría R a S), el cambio en el orden de prioridades (el grupo entrante tiene menor prioridad que el saliente pero altera el orden del cloro) hace que el descriptor estereoquímico se mantenga. Inversión espacial + Cambio de orden de prioridades $\rightarrow$ Configuración (R).
Pregunta 77
¿Cuál de los siguientes disolventes orgánicos es más denso que el agua a temperatura ambiente?:
- 1. Tetrahidrofurano.
- 2. Tolueno.
- 3. Diclorometano.
- 4. 2-cloro-metilpropano.
Explicación:
En las extracciones líquido-líquido, saber qué fase queda abajo (la más densa) es fundamental. El agua tiene una densidad aproximada de 1.00 g/mL.
- • Regla General:
- – La mayoría de los disolventes orgánicos (hidrocarburos, éteres, alcoholes, ésteres) son menos densos que el agua y flotan sobre ella (Fase superior).
- – Los disolventes halogenados (especialmente los polihalogenados) suelen ser más densos que el agua y se van al fondo (Fase inferior).
- • Análisis de las opciones:
- – Tetrahidrofurano (THF): Éter. Densidad ≈ 0.89 g/mL (Flota, aunque es miscible con agua si no se satura con sales).
- – Tolueno: Hidrocarburo aromático. Densidad ≈ 0.87 g/mL (Flota).
- – 2-cloro-2-metilpropano: Haluro de alquilo simple. Densidad ≈ 0.85 g/mL (Flota).
- – Diclorometano (CH2Cl2): Disolvente polihalogenado. Densidad ≈ 1.33 g/mL. Es significativamente más pesado que el agua.
Pregunta 78
¿Qué base favorece la formación del producto de Hofmann en una deshidrohalogenación de haluros terciarios por mecanismo E2?:
- 1. KOH.
- 2. NaOEt.
- 3. KOtBu.
- 4. NH3.
Explicación:
En una reacción de eliminación E2, la competencia entre la formación del alqueno más sustituido (Zaitsev) y el menos sustituido (Hofmann) depende principalmente del impedimento estérico.
- • Regla de Zaitsev vs. Hofmann:
- – Bases pequeñas (como OH–, MeO–, EtO–) pueden acceder a los protones internos más impedidos, formando el alqueno más estable (producto de Zaitsev).
- – Bases voluminosas (con gran impedimento estérico) tienen dificultad para acceder a los protones internos. Por ello, abstraen los protones más accesibles (externos o terminales), conduciendo al alqueno menos sustituido (producto de Hofmann).
- • Análisis de las opciones:
- – KOH y NaOEt (etóxido) son bases pequeñas; favorecen Zaitsev.
- – NH3 es una base débil, mala para E2.
- – KOtBu (t-butóxido de potasio): Es una base muy voluminosa. El grupo terc-butilo crea un gran impedimento estérico que impide la abstracción del protón más interno, favoreciendo casi exclusivamente la eliminación de Hofmann.
Pregunta 79
¿Cuál de los siguientes métodos permite obtener 1,2 dioles, en disposición relativa anti a partir de alquenos?:
- 1. Reacción con mCPBA y H2O/H+.
- 2. Reacción con OsO4.
- 3. Reacción con KMnO4.
- 4. Reacción con Br2.
Explicación:
La estereoquímica de la dihidroxilación (formación de dioles vecinales) depende del reactivo utilizado. Existen métodos para añadir los dos grupos -OH por la misma cara (syn) o por caras opuestas (anti).
- • Dihidroxilación Anti (Respuesta Correcta):
- – Ocurre en dos etapas. Primero, la reacción con un peroxiácido (como el mCPBA) forma un epóxido.
- – Segundo, la hidrólisis ácida (H2O/H+) abre el anillo de epóxido. El agua ataca por el lado opuesto al oxígeno del anillo (ataque dorsal tipo SN2), resultando en una disposición anti de los grupos hidroxilo.
- • Dihidroxilación Syn (Opciones Incorrectas):
- – Tanto el tetraóxido de osmio (OsO4) como el permanganato de potasio frío (KMnO4) forman un éster cíclico intermedio que transfiere ambos oxígenos a la misma cara del alqueno, produciendo dioles cis o syn.
- – La reacción con Br2 produce anti-dibromuros, no dioles.
Pregunta 80
El espectro de resonancia magnética nuclear de protón (1H-RMN) de un compuesto muestra la existencia de dos únicas señales: un doblete a 1,71 ppm y un septeto a 4,28 ppm. Ambas señales están acopladas entre sí con una constante de acoplamiento de aproximadamente 7 Hz. ¿Cuál de los siguientes compuestos podría corresponder con el espectro descrito?:
- 1. Dietil éter.
- 2. Acetato de etilo.
- 3. 2-bromopropano.
- 4. Tolueno.
Explicación:
El patrón de acoplamiento descrito (un doblete y un septeto) es la «huella dactilar» característica de un grupo isopropilo (-CH(CH3)2).
- • Análisis de Multiplicidad (Regla n + 1):
- – Los metilos (2 × CH3): Son 6 protones equivalentes vecinos a 1 solo protón (el del grupo CH). La señal se desdobla en 1 + 1 = 2 picos (Doblete).
- – El metino (CH): Es 1 protón vecino a 6 protones equivalentes (los de los metilos). La señal se desdobla en 6 + 1 = 7 picos (Septeto).
- • Análisis de Desplazamiento Químico (δ):
- – La señal a 4,28 ppm indica que el protón CH está unido a un átomo electronegativo (desapantallamiento), lo cual coincide con el bromo en posición alfa (α).
- – La señal a 1,71 ppm es típica de metilos con un grupo atractor de electrones en posición beta (β).
- • Descarte de otras opciones:
- – Dietil éter y Acetato de etilo: Tienen grupos etilo, que dan patrones de Triplete (CH3) y Cuartete (CH2).
- – Tolueno: Daría un singlete para el metilo y un multiplete aromático.
Pregunta 81
El aminoácido treonina (ácido 2-amino-3-hidroxibutanoico) tiene cuatro posibles estereoisómeros, representados a continuación. ¿Cuál de ellos es el que tiene configuración 2R,3R?:
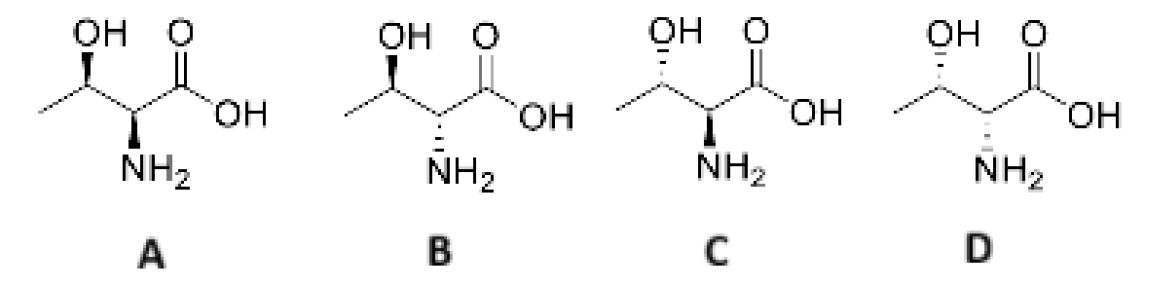
- 1. A.
- 2. B.
- 3. C.
- 4. D.
Explicación:
Para resolver la pregunta, debemos asignar la configuración absoluta (R/S) a los carbonos 2 y 3 de las estructuras propuestas utilizando las reglas de prioridad de Cahn-Ingold-Prelog.
- 1. Asignación de Prioridades:
- Carbono 2 (C2): -NH2 (1) > -COOH (2) > -CH(OH)CH3 (3) > -H (4).
- Carbono 3 (C3): -OH (1) > -CH(NH2)COOH (2) > -CH3 (3) > -H (4).
- 2. Análisis de la Estructura B (Opción 2):
- • Centro C2: El grupo -NH2 (prioridad 1) está en la posición trasera (línea discontinua) y el H (prioridad 4) hacia adelante. Estrategia: Hacemos un intercambio mental entre el grupo de atrás y el de adelante. Si analizamos la configuración resultante y la invertimos, obtendremos la real. O más simple: si el grupo de menor prioridad (H) está adelante, la configuración aparente se invierte. Sentido 1 → 2 → 3: (-NH2) → (-COOH) → (C3). Esto parece antihorario (S) desde nuestra perspectiva con el H delante, pero al aplicar la regla de inversión (o ver que el H apunta hacia nosotros), la configuración real es R. Resultado C2: 2R.
- • Centro C3: El grupo -OH (prioridad 1) está hacia adelante (cuña) y el H (prioridad 4) hacia atrás. Estrategia: El grupo de menor prioridad ya está atrás, así que leemos la configuración directamente. Sentido 1 → 2 → 3: (-OH) → (C2) → (-CH3). El giro es en el sentido de las agujas del reloj. Resultado C3: 3R.
Pregunta 82
Los dos protones en posición 3 del compuesto (R)-2-butanol son:
- 1. Homotópicos.
- 2. Enantiotópicos.
- 3. Racémicos.
- 4. Diastereotópicos.
Explicación:
Para determinar la relación entre dos átomos (o grupos) idénticos en una molécula, aplicamos el criterio de sustitución: sustituimos mentalmente cada uno de los protones por un grupo diferente (Z) y comparamos los productos resultantes.
- • Análisis del (R)-2-butanol:
- – La molécula ya posee un centro quiral preexistente en el carbono 2 (configuración R).
- – Los protones en cuestión están en el carbono 3 (-CH2-).
- • Criterio de Sustitución:
- – Si sustituimos el protón Ha, se crea un nuevo centro quiral en C3. El producto tendría, por ejemplo, configuración (2R, 3R).
- – Si sustituimos el protón Hb, el producto tendría la configuración opuesta en el nuevo centro, es decir, (2R, 3S).
- – La relación entre (2R, 3R) y (2R, 3S) no es de enantiómeros (imágenes especulares), sino de diastereoisómeros (difieren en la configuración de al menos un centro, pero no de todos).
Pregunta 83
La reacción de Michael entre acetoacetato de etilo y 3-buten-2-ona que se muestra a continuación. ¿Cuál es el producto mayoritario de esta reacción?:
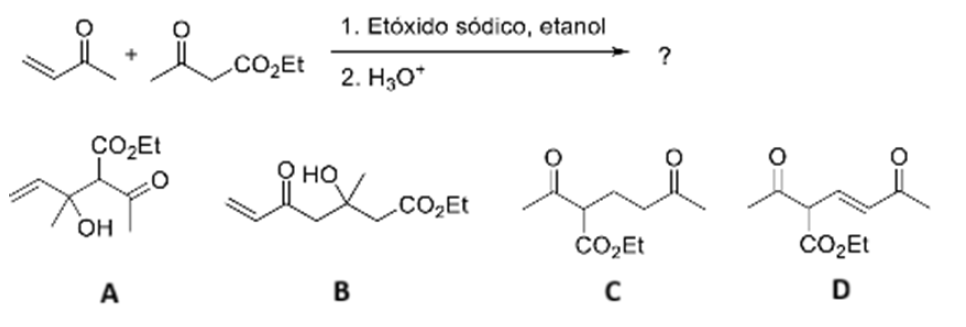
- 1. A.
- 2. B.
- 3. C.
- 4. D.
Explicación:
La reacción mostrada es una Adición de Michael, que consiste en la adición nucleófila conjugada de un enolato a un sistema α,β-insaturado.
- • Formación del Nucleófilo (Donador de Michael):
- – El etóxido sódico actúa como base y desprotona el carbono α del acetoacetato de etilo (el carbono central entre los dos grupos carbonilo), que es la posición más ácida.
- – Esto genera un enolato estabilizado por resonancia.
- • Ataque Nucleófilo (Aceptor de Michael):
- – El enolato ataca al carbono β (posición 4) de la 3-buten-2-ona (metil vinil cetona) mediante una adición 1,4.
- – La adición de Michael es termodinámicamente favorable frente a la adición directa (1,2) al carbonilo.
- • Producto Final:
- – Tras el tratamiento ácido (H3O+), el enolato intermedio se protona para dar un compuesto tricarbonílico saturado (un compuesto 1,5-dicarbonílico).
- – La estructura C muestra correctamente la unión entre el carbono central del acetoacetato y el extremo de la cadena de la cetona, manteniendo todos los grupos funcionales intactos.
Pregunta 84
La oxidación de Baeyer-Villiger de ciclohexanona con ácido m-cloroperoxibenzoico (mCPBA) da como producto principal:
- 1. Ácido hexanoico.
- 2. Caprolactama.
- 3. ε-Caprolactona.
- 4. Ciclohexanol.
Explicación:
La oxidación de Baeyer-Villiger consiste en la transformación de una cetona en un éster mediante la inserción de un átomo de oxígeno, utilizando un peroxiácido (como el mCPBA).
- • Reacción en Cetonas Cíclicas (Expansión de Anillo):
- – Cuando el reactivo es una cetona cíclica, la inserción del oxígeno ocurre adyacente al carbonilo, expandiendo el anillo en una unidad.
- – El producto resultante es un éster cíclico, denominado genéricamente lactona.
- • Caso de la Ciclohexanona:
- – Partimos de un anillo de 6 miembros (Ciclohexanona).
- – Al insertar el oxígeno, se forma un anillo de 7 miembros.
- – Este compuesto es la ε-caprolactona (o 2-oxepanona).
- • Diferenciación de opciones:
- – Caprolactama (Opción 2): Es la amida cíclica análoga, pero se obtiene mediante la Transposición de Beckmann de la oxima de la ciclohexanona, no por oxidación directa.
Pregunta 85
Considerando los siguientes potenciales estándar de oxidación: Cl2/Cl– (E⁰ = 1,36 V), I2/I– (E⁰ = 0,54 V) y Fe3+/Fe2+ (E⁰ = 0,77 V), indique cuál de las siguientes afirmaciones es VERDADERA:
- 1. El Fe3+ puede oxidar al Cl–.
- 2. El I2 y el Cl2 pueden oxidar al Fe2+ a Fe3+.
- 3. El I2 puede oxidar al Fe2+ a Fe3+.
- 4. El Cl2 puede oxidar al Fe2+ a Fe3+.
Explicación:
Esta pregunta fue IMPUGNADA debido a un error fundamental en la terminología de los datos proporcionados.
- • El Error del Enunciado:
- – El texto habla de «potenciales estándar de oxidación«, pero proporciona los valores de los potenciales estándar de reducción (Cl2 → Cl– es +1,36 V).
- – Si fueran realmente potenciales de oxidación, los signos deberían estar invertidos o las reacciones ser opuestas. Esta contradicción invalida la pregunta desde un punto de vista riguroso.
- • Análisis Químico (Asumiendo Potenciales de Reducción):
- – Para que una reacción redox sea espontánea, el oxidante debe tener un potencial de reducción mayor que el par redox que se va a oxidar.
- – Orden de fuerza oxidante (mayor E⁰): Cl2 (1,36 V) > Fe3+ (0,77 V) > I2 (0,54 V).
- – Opción 4: El Cl2 (1,36 V) tiene mayor potencial que el par Fe3+/Fe2+ (0,77 V). Por tanto, el Cl2 puede oxidar espontáneamente al Fe2+ (E⁰celda = 1,36 – 0,77 = +0,59 V).
- – Bajo la interpretación estándar, la 4 sería correcta, pero el error de enunciado obligó a su anulación.
Pregunta 86
En un análisis gravimétrico, ¿qué propiedad del analito se mide indirectamente?:
- 1. Su absorbancia.
- 2. Su masa.
- 3. Su potencial electroquímico.
- 4. Su conductividad.
Explicación:
El análisis gravimétrico es un método cuantitativo que se basa en la medición precisa de la masa.
- • ¿Por qué indirectamente?
- – Rara vez se aísla y pesa el analito en su forma original pura.
- – Lo habitual es convertir el analito (mediante reacciones de precipitación o volatilización) en un compuesto de composición química conocida y estable (ej. pesar AgCl para determinar Cl–).
- – A partir de la masa de este compuesto medido en la balanza, se calcula matemáticamente (indirectamente) la masa del analito original usando factores gravimétricos.
- • Descarte de opciones:
- – Absorbancia: Espectroscopía.
- – Potencial: Potenciometría.
- – Conductividad: Conductimetría.
Pregunta 87
¿Qué tipo de electrodo indicador se usa habitualmente para medir el pH en soluciones acuosas?:
- 1. Electrodo de platino.
- 2. Electrodo de vidrio.
- 3. Electrodo de plata.
- 4. Electrodo de mercurio.
Explicación:
La medición potenciométrica del pH requiere un electrodo indicador cuya respuesta dependa selectivamente de la actividad de los iones hidronio (H3O+).
- • Electrodo de Vidrio (Respuesta Correcta):
- – Es un electrodo de membrana selectiva de iones (ISE).
- – Posee una fina membrana de vidrio de composición especial (silicatos dopados) que permite el intercambio iónico superficial con los protones de la disolución.
- – La diferencia de potencial generada a través de la membrana sigue la ecuación de Nernst y es proporcional al pH. Es el estándar universal en laboratorios.
- • Descarte de otros electrodos:
- – Platino: Electrodo inerte metálico, usado para medir potenciales redox generales.
- – Plata: Electrodo metálico de primera especie, sensible a la actividad de Ag+ (o de segunda especie como Ag/AgCl para referencia).
- – Mercurio: Históricamente usado en polarografía (electrodo de gotas), no para pH.
Pregunta 88
En la cromatografía de exclusión molecular, ¿qué solutos eluirán primero?:
- 1. Los de mayor tamaño.
- 2. Los de menor tamaño.
- 3. Los más ácidos.
- 4. Los más básicos.
Explicación:
La cromatografía de exclusión molecular (también llamada filtración en gel o permeación en gel) separa las moléculas basándose exclusivamente en su tamaño efectivo en solución (volumen hidrodinámico).
- • Mecanismo de separación:
- – La columna está rellena de partículas porosas con cavidades de tamaño definido.
- – Moléculas Pequeñas (Se retienen): Son capaces de penetrar en los poros de la fase estacionaria. Al entrar y salir de estos «laberintos», recorren un camino mucho más largo, lo que retrasa su salida (mayor tiempo de retención).
- – Moléculas Grandes (Eluyen primero): Son demasiado grandes para entrar en los poros («exclusión»). Solo pueden circular por el volumen intersticial (el espacio entre las partículas). Al no desviarse dentro de los poros, recorren el camino más corto y salen de la columna más rápidamente.
Pregunta 89
En los instrumentos de análisis, ¿qué dispositivo convierte una magnitud física en una señal eléctrica?:
- 1. Transductor de entrada.
- 2. Amplificador.
- 3. Potenciómetro.
- 4. Detector óptico.
Explicación:
En un instrumento analítico moderno, el flujo de información generalmente sigue el esquema: Estímulo → Muestra → Respuesta → Transductor → Procesamiento → Lectura.
- • Definición de Transductor de Entrada (Input Transducer):
- – Es el componente crítico que convierte la información de un dominio no eléctrico (químico o físico, como intensidad de luz, pH, temperatura, masa) a un dominio eléctrico (corriente, voltaje, frecuencia).
- – Esta conversión es necesaria para que la señal pueda ser amplificada, digitalizada y procesada por los circuitos electrónicos del instrumento.
- • Análisis de las opciones:
- – Amplificador: Aumenta la magnitud de la señal eléctrica ya existente, no realiza la conversión inicial de energía.
- – Potenciómetro: Es un componente de circuito (resistencia variable), no un conversor de dominio general.
- – Detector óptico: Es un tipo específico de transductor (luz a electricidad), pero la pregunta pide el nombre genérico del dispositivo para cualquier magnitud física.
Pregunta 90
En una célula electroquímica galvánica, ¿qué ocurre en el ánodo?:
- 1. Tiene lugar una reacción de reducción.
- 2. Se generan aniones a partir del metal neutro del propio ánodo.
- 3. Se reciben los electrones que proceden del cátodo.
- 4. Tiene lugar una reacción de oxidación.
Explicación:
En electroquímica, la definición de los electrodos se basa estrictamente en el tipo de semirreacción que ocurre en ellos.
- • Regla General (Ánodo-Oxidación):
- – El Ánodo es siempre el electrodo donde ocurre la Oxidación (pérdida de electrones). Regla mnemotécnica: Vocal con Vocal (Anodo – Oxidación).
- – El Cátodo es donde ocurre la Reducción (ganancia de electrones). Regla mnemotécnica: Consonante con Consonante (Cátodo – Reducción).
- • Análisis de las opciones incorrectas:
- – Opción 2: En la oxidación de un metal anódico ($M \rightarrow M^{n+} + ne^-$), se generan cationes que pasan a la disolución, no aniones.
- – Opción 3: En una pila galvánica, el ánodo es el polo negativo y es la fuente de electrones; los electrones salen del ánodo hacia el circuito externo, no se reciben allí.
Pregunta 91
¿Cuál es el orden correcto de las etapas del proceso analítico?:
- 1. Selección del método de análisis → Definición del problema → Medida de la señal analítica → Obtención de la muestra → Tratamiento de la muestra → Evaluación de los resultados y elaboración del informe.
- 2. Medida de la señal analítica → Definición del problema → Selección del método de análisis → Obtención de la muestra → Tratamiento de la muestra → Evaluación de los resultados y elaboración del informe.
- 3. Definición del problema → Selección del método de análisis → Obtención de la muestra → Tratamiento de la muestra → Medida de la señal analítica → Evaluación de los resultados y elaboración del informe.
- 4. Definición del problema → Obtención de la muestra → Selección del método de análisis → Medida de la señal analítica → Evaluación de los resultados y elaboración del informe → Tratamiento de la muestra.
Explicación:
El proceso analítico es una secuencia lógica de pasos diseñada para obtener información química de calidad sobre la materia. El orden es inalterable por necesidad lógica:
- 1. Definición del Problema: Antes de nada, se debe saber qué se busca (¿qué analito?, ¿cuánta precisión?, ¿cuánto tiempo hay?).
- 2. Selección del Método: Basándose en lo anterior, se elige la técnica adecuada (gravimetría, espectroscopía, cromatografía, etc.).
- 3. Obtención de la Muestra (Muestreo): Se toma una porción representativa del lote.
- 4. Tratamiento de la Muestra: Preparación previa (disolución, eliminación de interferencias, preconcentración) para que sea apta para el instrumento.
- 5. Medida de la Señal: Ejecución experimental para obtener datos brutos.
- 6. Evaluación y Informe: Procesamiento estadístico de datos, interpretación y comunicación de resultados.
Pregunta 92
¿Qué determina principalmente la selectividad de un método analítico?:
- 1. El tipo de matriz.
- 2. Los interferentes de la muestra.
- 3. La cantidad de la muestra.
- 4. La concentración del analito de interés.
Explicación:
La selectividad es un parámetro de calidad (cifra de mérito) que describe la capacidad de un método para medir con exactitud y especificidad el analito de interés en presencia de otros componentes.
- • Definición y Causa:
- – Un método es selectivo si puede distinguir el analito de otras especies químicas presentes en la muestra.
- – Estas «otras especies» que generan una señal indistinguible a la del analito o que alteran su medición se denominan interferentes. Por tanto, la selectividad se define y se mide en función de la capacidad del método para tolerar estos interferentes.
- • Coeficiente de Selectividad:
- – Matemáticamente, la selectividad se cuantifica mediante coeficientes que relacionan la respuesta del interferente (I) con la del analito (A). Sin la presencia de interferentes, el concepto de selectividad no tendría objeto de evaluación crítica.
- • Descarte de otras opciones:
- – La matriz es el conjunto total, pero es la presencia específica de interferentes dentro de ella lo que desafía la selectividad.
- – La cantidad de muestra o concentración afectan a la sensibilidad o al límite de detección, no a la selectividad.
Pregunta 93
En la cromatografía líquida de alta resolución (HPLC), ¿qué parámetro describe la retención relativa de un soluto respecto a otro?:
- 1. Número de platos teóricos (N).
- 2. Factor de capacidad (k’).
- 3. Factor de selectividad (α).
- 4. Volumen de retención (Vr).
Explicación:
Para evaluar la separación entre dos picos cromatográficos, es necesario comparar cómo se retienen entre sí.
- • Factor de Selectividad (α) [Respuesta Correcta]:
- – Describe la capacidad de un sistema cromatográfico para discriminar entre dos compuestos.
- – Se define matemáticamente como el cociente entre los factores de capacidad (o retención) de dos solutos, siendo siempre mayor o igual a 1.
- – Al ser un cociente, representa la retención relativa del soluto B respecto al soluto A.
- • Descarte de otros parámetros:
- – Factor de capacidad (k’): Mide la retención de un único soluto en relación con el tiempo muerto.
- – Platos teóricos (N): Mide la eficiencia de la columna (anchura del pico), no la separación relativa entre picos.
Pregunta 94
¿Cuál de los siguientes enunciados es VERDADERO?:
- 1. La curva de calibración es la gráfica que representa la respuesta analítica en función de la concentración del analito correspondiente.
- 2. La disolución patrón o estándar es una disolución de concentración desconocida.
- 3. El error sistemático varía de forma aleatoria al repetir la medida.
- 4. El error aleatorio se repite de manera constante.
Explicación:
Analicemos la veracidad de cada afirmación basándonos en los fundamentos de la química analítica:
- • Opción 1 (Verdadera):
- – La curva de calibrado es, por definición, la representación gráfica de la señal medida (eje Y) frente a concentraciones conocidas del analito (eje X). Permite interpolar la concentración de muestras desconocidas.
- • Análisis de las opciones falsas:
- – Opción 2: Una disolución patrón (estándar) tiene, necesariamente, una concentración conocida con exactitud.
- – Opción 3: El error sistemático es constante o varía de forma predecible (sesgo), afectando a la exactitud. No varía aleatoriamente.
- – Opción 4: El error aleatorio (indeterminado) fluctúa de forma impredecible en cada medida, afectando a la precisión. No es constante.
Pregunta 95
El blanco o una disolución del blanco contiene:
- 1. Los reactivos y disolventes que se utilizan en una determinación.
- 2. El analito de interés.
- 3. El analito de interés y los reactivos que se utilizan en una determinación.
- 4. El analito de interés, los reactivos y disolventes que se utilizan en una determinación.
Explicación:
En química analítica, el blanco es una referencia fundamental para asegurar la exactitud de la medida.
- • Definición de Blanco de Método:
- – Es una disolución que contiene todos los componentes (disolventes, ácidos de digestión, reactivos colorimétricos, tampones, etc.) que se añaden a la muestra desconocida durante el análisis.
- – La característica clave es que NO contiene el analito de interés.
- • Función:
- – Permite medir la señal generada por los reactivos y el entorno (absorbancia de fondo, impurezas en los reactivos).
- – Esta señal se resta a la señal de la muestra para obtener la respuesta neta debida exclusivamente al analito.
- • Descarte de opciones:
- – Cualquier opción que incluya «el analito de interés» (2, 3 y 4) se refiere a un patrón o estándar, no a un blanco.
Pregunta 96
¿Cuál es la principal ventaja que presenta la espectrometría de masas que utiliza la técnica MALDI (ionización/desorción por láser asistida por matriz) como fuente de desorción-ionización de la muestra?:
- 1. Permite la detección directa de gases inorgánicos ligeros.
- 2. No precisa de una matriz que absorba de manera intensa el láser.
- 3. Utiliza exclusivamente iones negativos para mejorar la resolución.
- 4. Permite analizar biomoléculas grandes como proteínas o polímeros sin fragmentación significativa.
Explicación:
La técnica MALDI (Matrix-Assisted Laser Desorption/Ionization) revolucionó la espectrometría de masas al permitir el análisis de macromoléculas no volátiles y térmicamente inestables.
- • Ionización Suave (Soft Ionization):
- – A diferencia de técnicas «duras» como el Impacto Electrónico (EI), que rompen la molécula, el MALDI utiliza pulsos láser sobre una matriz cristalina.
- – La matriz absorbe la energía del láser y la transfiere suavemente al analito, provocando su desorción e ionización (generalmente como [M+H]+) con una energía interna mínima.
- – Esto permite observar el ion molecular intacto de proteínas gigantes (hasta 300-500 kDa), ADN y polímeros sintéticos sin que se fragmenten en pedazos pequeños.
- • Análisis de las opciones incorrectas:
- – Opción 2: Es falso; la técnica requiere obligatoriamente una matriz que absorba la longitud de onda del láser (ej. ácido sinapínico).
- – Opción 3: Funciona tanto en modo positivo como negativo.
Pregunta 97
¿Qué componentes del espectrómetro de masas son el cuadrupolo y el tiempo de vuelo (TOF)?:
- 1. Sistemas de introducción de la muestra.
- 2. Analizadores de masas.
- 3. Fuentes de ionización.
- 4. Detectores.
Explicación:
Un espectrómetro de masas consta de tres bloques fundamentales: Fuente de Ionización → Analizador de Masas → Detector.
- • Función del Analizador de Masas:
- – Es el «corazón» del instrumento. Su función es separar los iones generados en la fuente en función de su relación masa/carga ($m/z$).
- • Tipos mencionados en la pregunta:
- – Cuadrupolo (Quadrupole): Utiliza campos eléctricos oscilantes (radiofrecuencia y corriente continua) aplicados a cuatro barras paralelas para filtrar los iones. Solo los iones con un $m/z$ específico tienen una trayectoria estable y atraviesan el dispositivo en un momento dado.
- – Tiempo de Vuelo (Time of Flight – TOF): Acelera todos los iones con la misma energía cinética hacia un tubo libre de campos. Los iones más ligeros viajan más rápido y llegan antes al detector que los pesados. La masa se determina midiendo el tiempo que tardan en «volar» hasta el detector.
- • Descarte de otras opciones:
- – Fuentes de ionización: Son dispositivos como el Impacto Electrónico (EI), Electrospray (ESI) o MALDI.
- – Detectores: Son dispositivos como el multiplicador de electrones o la copa de Faraday.
Pregunta 98
¿Qué tipo de error es causado consistentemente por un mismo factor, desplazando los resultados en una misma dirección?:
- 1. Error aleatorio.
- 2. Error sistemático.
- 3. Error total.
- 4. Error casual.
Explicación:
En el análisis de datos experimentales, los errores se clasifican según su naturaleza y su efecto en los resultados.
- • Error Sistemático (o Determinado):
- – Tiene un valor definido y una causa asignable (ej. una pipeta mal calibrada que siempre entrega 0,1 mL menos).
- – Es unidireccional: siempre desvía los resultados en el mismo sentido (sesgo), haciendo que la media de las mediciones difiera del valor verdadero.
- – Afecta a la exactitud del método.
- • Error Aleatorio (o Casual/Indeterminado):
- – Es causado por múltiples variables incontrolables que fluctúan al azar.
- – Se distribuye en ambas direcciones (positivo y negativo) alrededor de la media, siguiendo una distribución normal (Gaussiana).
- – Afecta a la precisión (reproducibilidad), pero tiende a cancelarse al aumentar el número de medidas ($N$).
Pregunta 99
En la garantía de calidad analítica, un material estándar de referencia se utiliza para:
- 1. Verificar la exactitud de los resultados.
- 2. Ajustar el volumen de las muestras antes del análisis.
- 3. Determinar el límite de detección de un método.
- 4. Verificar la precisión de los resultados.
Explicación:
Un Material de Referencia Estándar (SRM) o Certificado (CRM) es un material suficientemente homogéneo y estable con respecto a una o más propiedades, las cuales han sido establecidas con un alto nivel de confianza.
- • Propósito Principal: Exactitud (Veracidad):
- – La exactitud mide la cercanía del valor experimental al valor verdadero o aceptado.
- – Dado que el SRM tiene un «valor verdadero» conocido (certificado), es la herramienta patrón para evaluar el sesgo o error sistemático del método. Si el análisis del SRM arroja el valor certificado, el método es exacto.
- • Diferencia con Precisión:
- – La precisión (repetibilidad/reproducibilidad) se evalúa midiendo repetidamente cualquier muestra homogénea, no necesariamente un costoso estándar de referencia.
Pregunta 100
¿Qué parámetro estadístico se utiliza para expresar el rango dentro del cual se espera encontrar el valor verdadero con cierta probabilidad?:
- 1. Error total.
- 2. Media aritmética.
- 3. Intervalo de confianza.
- 4. Varianza.
Explicación:
En estadística inferencial, rara vez podemos conocer el «valor verdadero» (μ) de una población con una sola medida. Por ello, expresamos nuestros resultados como un rango de valores probables.
- • Definición de Intervalo de Confianza (IC):
- – Es el rango de valores, calculado a partir de los datos de una muestra, en el que se confía que se encuentre el parámetro poblacional verdadero con una probabilidad específica (el nivel de confianza, habitualmente 95% o 99%).
- – Su fórmula general se expresa como:μ = x̄ ± (ts / √N) (Donde x̄ es la media, s la desviación estándar, N el número de medidas y t el valor de Student).
- • Descarte de otras opciones:
- – Media aritmética: Es una estimación puntual, un solo valor, no un rango.
- – Varianza: Mide la dispersión de los datos al cuadrado, no la localización del valor verdadero.
Pregunta 101
En la validación de un método instrumental, el límite de detección se define como:
- 1. La concentración más alta que puede medirse con exactitud.
- 2. La menor concentración de analito que es significativamente distinta del ruido de fondo.
- 3. 10 veces la desviación estándar de las medidas repetitivas realizadas sobre el blanco.
- 4. La diferencia de señal entre dos concentraciones sucesivas en una curva de calibrado.
Explicación:
El Límite de Detección (LOD) es el parámetro que indica la capacidad del método para distinguir una señal real del «ruido» aleatorio del instrumento.
- • Definición Conceptual (Opción 2):
- – Es la cantidad o concentración mínima de sustancia que puede ser detectada con fiabilidad (es decir, podemos decir «sí, está presente»), aunque no necesariamente cuantificada con exactitud.
- – Esto ocurre cuando la señal supera un umbral crítico por encima del ruido de fondo (señal/ruido ≥ 3).
- • Diferencia con el Límite de Cuantificación (LOQ):
- – LOD (Detección): Matemáticamente se suele estimar como la señal del blanco más 3 veces su desviación estándar (3σ).
- – LOQ (Cuantificación): Es la menor cantidad que se puede medir con precisión aceptable. Se estima como la señal del blanco más 10 veces su desviación estándar (10σ). Por tanto, la opción 3 define el LOQ, no el LOD.
- • Otras opciones:
- – La opción 1 se refiere al límite superior de linealidad (LOL).
- – La opción 4 describe la sensibilidad de calibración.
Pregunta 102
En cuanto a los parámetros ondulatorios, ¿qué es la longitud de onda?:
- 1. Es la longitud del vector electrónico en la altura máxima del pico.
- 2. Es el tiempo en segundos necesario para el paso de máximos o mínimos sucesivos por un punto fijo del espacio.
- 3. Es el número de oscilaciones de la forma de onda en 1 segundo.
- 4. Es la distancia lineal entre dos puntos equivalentes cualesquiera de una onda sucesiva.
Explicación:
Para describir una onda electromagnética, se utilizan varios parámetros interrelacionados. Identifiquemos a qué corresponde cada opción:
- • Longitud de Onda (λ) [Opción 4]:
- – Se define como la distancia física (en metros, nanómetros, etc.) entre dos picos (crestas) sucesivos, dos valles sucesivos o, más genéricamente, entre dos puntos idénticos en ciclos consecutivos de la onda.
- • Análisis de las otras opciones:
- – Opción 1 (Amplitud): La altura del pico respecto al punto de equilibrio se relaciona con la intensidad de la radiación, no con su longitud.
- – Opción 2 (Periodo, T): Es una medida de tiempo, no de distancia. Es el tiempo que tarda la onda en completar un ciclo.
- – Opción 3 (Frecuencia, ν): Es la inversa del periodo (1/T). Representa la cantidad de ciclos que ocurren por unidad de tiempo (Hertz).
Pregunta 103
¿Qué expresa el producto de solubilidad (Kps) de una sal ligeramente soluble?:
- 1. La suma de las concentraciones de todos los iones.
- 2. El producto de las concentraciones molares de los iones en equilibrio, cada una elevada a su coeficiente estequiométrico.
- 3. La masa disuelta por litro.
- 4. El pH de la disolución saturada.
Explicación:
El producto de solubilidad (Kps o Ksp) es la constante de equilibrio que se aplica a la disolución de un compuesto iónico poco soluble en agua.
- • Definición Termodinámica:
- – Para una sal genérica que se disocia según la ecuación: AmBn (s) ↔ m An+ (aq) + n Bm- (aq)
- – La Ley de Acción de Masas establece que, en una disolución saturada (equilibrio), el producto de las concentraciones de los iones es constante a una temperatura dada.
- • Expresión Matemática:
- – La expresión se construye multiplicando las concentraciones molares de los productos (iones), elevando cada una al número de moles que aparecen en la ecuación ajustada (coeficiente estequiométrico). Kps = [An+]m ċ [Bm-]n
- (Nota: La concentración del sólido puro no se incluye porque su actividad es constante = 1).
- • Descarte de otras opciones:
- – La masa disuelta por litro es la solubilidad (s), no la constante Kps.
Pregunta 104
Se tiene una disolución reguladora en la que la concentración de la forma ácida es dos órdenes de magnitud superior a la de la forma básica conjugada. De acuerdo con la ecuación de Henderson-Hasselbalch, el pH de la disolución es:
- 1. pH = pKa
- 2. pH = pKa + 2
- 3. pH = pKa – 2
- 4. pH = 2pKa
Explicación:
Para resolver este problema, aplicamos directamente la ecuación fundamental de los sistemas amortiguadores (buffers).
- 1. Ecuación de Henderson-Hasselbalch:pH = pKa + log ( [Base] / [Ácido] )
- 2. Interpretación del Enunciado:
- – «La concentración de la forma ácida es dos órdenes de magnitud superior a la básica».
- – Matemáticamente: [Ácido] = 100 × [Base].
- – Por tanto, la relación [Base] / [Ácido] es igual a 1 / 100 (o 10-2).
- 3. Sustitución y Cálculo:
- pH = pKa + log(10-2)
- Como el logaritmo en base 10 de 10-2 es -2:
- pH = pKa – 2
Pregunta 105
Indique cuál de las siguientes afirmaciones relacionadas con la ley de Lambert – Beer es VERDADERA:
- 1. La transmitancia es proporcional a la concentración de la especie absorbente.
- 2. La ley sólo es aplicable, de forma general, hasta una concentración máxima igual a 0,01 M.
- 3. El coeficiente de extinción molar depende únicamente de la naturaleza química de la especie absorbente.
- 4. La medida analítica se puede hacer en cualquier longitud de onda con la misma sensibilidad.
Explicación:
La Ley de Beer-Lambert (A = ε·b·C) describe una relación lineal ideal entre la absorbancia y la concentración, pero esta linealidad tiene límites físicos y químicos.
- • Limitaciones Reales (Opción 2 – Verdadera):
- – A concentraciones altas (generalmente > 0,01 M), las moléculas absorbentes están tan cerca unas de otras que sus nubes electrónicas interactúan.
- – Estas interacciones alteran su capacidad de absorber luz a una longitud de onda dada (ε cambia), provocando desviaciones negativas de la linealidad. Por tanto, la ley es estrictamente válida solo para disoluciones diluidas (≤ 0,01 M).
- • Análisis de las opciones falsas:
- – Opción 1: La absorbancia (A) es proporcional a la concentración, pero la transmitancia (T) disminuye exponencialmente (T = 10-A).
- – Opción 3: El coeficiente de extinción molar (ε) depende de la especie química, pero también fuertemente de la longitud de onda, el disolvente y la temperatura.
- – Opción 4: La sensibilidad depende del valor de ε. Para máxima sensibilidad, se debe medir en el máximo de absorción (λmax).
Pregunta 106
El intervalo dinámico de un método analítico se extiende desde:
- 1. El límite de cuantificación hasta el límite de linealidad.
- 2. El límite de detección hasta el límite de cuantificación.
- 3. El límite de linealidad hasta el límite de detección.
- 4. El blanco hasta el límite de linealidad.
Explicación:
Para validar un método cuantitativo, es crucial definir en qué rango de concentraciones los resultados son fiables. Esto se define mediante el Intervalo Dinámico Lineal.
- • Definición de los Límites:
- – Límite de Detección (LOD): Se detecta la presencia del analito, pero el error es demasiado grande para cuantificarlo (Región de detección cualitativa).
- – Límite de Cuantificación (LOQ): Es la concentración mínima a partir de la cual se puede medir el analito con una precisión y exactitud aceptables. Aquí empieza la zona útil.
- – Límite de Linealidad (LOL): Es la concentración máxima hasta la cual la respuesta del instrumento sigue una relación lineal con la concentración. Por encima de este punto, la curva se desvía.
- • El Intervalo Dinámico (Lineal):
- – Es el rango de concentraciones donde el método puede utilizarse para determinaciones cuantitativas directas sin necesidad de diluir la muestra.
- – Matemáticamente y por definición en guías de validación (como la ICH), este intervalo abarca desde el LOQ hasta el LOL.
Pregunta 107
¿Qué ley relaciona la solubilidad de un gas con su presión parcial sobre la disolución?:
- 1. Ley de Raoult.
- 2. Ley de Dalton.
- 3. Ley de Henry.
- 4. Ley de Hess.
Explicación:
El comportamiento de los gases disueltos en líquidos se describe fundamentalmente mediante la Ley de Henry.
- • Enunciado de la Ley de Henry (Opción 3):
- – Establece que, a una temperatura constante, la cantidad de gas disuelto en un volumen determinado de líquido es directamente proporcional a la presión parcial de ese gas en equilibrio con el líquido.
- – Matemáticamente: C = kH · P(Donde C es la concentración del gas disuelto, P es la presión parcial del gas y kH es la constante de Henry, específica para cada gas, disolvente y temperatura).
- – Ejemplo cotidiano: Al abrir una bebida gaseosa, la presión disminuye drásticamente y, según la ley de Henry, la solubilidad del CO2 baja, provocando que el gas escape en forma de burbujas.
- • Descarte de otras opciones:
- – Ley de Raoult: Relaciona la presión de vapor de un disolvente en una disolución con su fracción molar (propiedades coligativas).
- – Ley de Dalton: Trata sobre las presiones parciales en mezclas de gases (Ptotal = ∑ Pi), no sobre solubilidad.
- – Ley de Hess: Es una ley termoquímica sobre la aditividad de las entalpías de reacción.
Pregunta 108
¿Qué condición debe cumplir un indicador en una valoración ácido-base?:
- 1. El color del indicador debe ser el mismo que el del analito.
- 2. El viraje de color del indicador debe darse en las proximidades del punto de equivalencia.
- 3. El rango de pH del indicador debe coincidir con el valor de pKa de la especie a valorar.
- 4. La indicación del punto final está basada en la aparición de turbidez.
Explicación:
El objetivo de una valoración es determinar el punto exacto donde la reacción química se completa (punto de equivalencia). El indicador es la herramienta visual que nos avisa de este momento (punto final).
- • La Condición Fundamental (Opción 2):
- – En el punto de equivalencia, se produce un cambio brusco (salto) de pH.
- – Para que el error de valoración sea despreciable, el intervalo de viraje del indicador (el rango de pH donde cambia de color) debe estar comprendido dentro de la parte vertical de la curva de valoración.
- – Es decir, el cambio de color debe ocurrir lo más cerca posible del pH del punto de equivalencia.
- • Por qué la Opción 3 es falsa:
- – Si valoramos un ácido débil (pKa ácido) con una base fuerte, en el punto de equivalencia se forma una base débil, por lo que el pH será básico (> 7).
- – Si eligiéramos un indicador con un pKa igual al del ácido (ácido), viraría mucho antes de llegar a la equivalencia. El pKa del indicador debe coincidir con el pH del punto de equivalencia, no con el pKa del analito.
Pregunta 109
¿Qué función cumple el almidón en una valoración redox en la que se emplea yodo?:
- 1. Actúa como un agente reductor en la reacción de oxidación del yodo.
- 2. Actúa como un catalizador en la reacción de titulación del yodo.
- 3. Actúa como un agente oxidante en la formación del complejo de yodo.
- 4. Actúa como un indicador visual del punto final de la titulación al formar un complejo de color azul intenso con el yodo.
Explicación:
En las valoraciones que involucran yodo (iodimetrías y iodometrías), el propio yodo tiene color (amarillo-pardo), pero en disoluciones diluidas este color es demasiado pálido para detectar el punto final con precisión.
- • Mecanismo de Indicación (Opción 4):
- – El almidón es un polímero de glucosa compuesto por amilosa y amilopectina.
- – La fracción de amilosa forma una estructura helicoidal en disolución. Las moléculas de yodo (en forma de ion triyoduro, $I_3^-$) se introducen en el interior de esta hélice formando un complejo de inclusión (clatrato).
- – Este complejo absorbe luz visible de tal manera que presenta un color azul oscuro intenso, visible incluso a concentraciones micromolares de yodo.
- • Aplicación Práctica:
- – Iodimetría (Directa): El punto final se marca por la aparición del color azul (exceso de $I_2$).
- – Iodometría (Indirecta): El punto final se marca por la desaparición del color azul. (Nota: Se añade cerca del final para evitar que el yodo quede atrapado irreversiblemente en el almidón).
Pregunta 110
¿Cuál de las siguientes técnicas de tratamiento de muestra sería la más indicada para el análisis cuantitativo de metales en una muestra sólida?:
- 1. Extracción en fase sólida.
- 2. Digestión asistida por microondas.
- 3. Extracción líquido-líquido.
- 4. Extracción con fluidos supercríticos.
Explicación:
Para cuantificar el contenido total de metales en una matriz sólida mediante técnicas espectroscópicas (como absorción atómica o ICP-MS), es necesario llevar los metales a una disolución líquida.
- • Digestión Asistida por Microondas (Opción 2):
- – Es el método estándar de referencia («Gold Standard»).
- – Consiste en tratar la muestra sólida con ácidos fuertes (HNO3, HCl, HF) dentro de recipientes cerrados expuestos a radiación de microondas.
- – La energía de microondas calienta la mezcla de forma rápida y eficiente, alcanzando altas presiones y temperaturas que destruyen (mineralizan) completamente la matriz orgánica o inorgánica, liberando los metales y dejándolos en solución para su análisis posterior.
- • Por qué se descartan las otras opciones (Técnicas de Separación):
- – Extracción en Fase Sólida (SPE) y Líquido-Líquido (LLE): Se utilizan para separar o purificar analitos que ya están disueltos en una fase líquida. No sirven para descomponer un sólido.
- – Fluidos Supercríticos (SFE): Se utiliza principalmente para extraer compuestos orgánicos no polares (grasas, pesticidas). La extracción de metales requiere complejantes específicos y no es la técnica de elección para cuantificación total.
Pregunta 111
¿Cuál de las siguientes afirmaciones describe una ventaja de la microextracción en fase sólida (SPME)?:
- 1. Requiere grandes volúmenes de disolvente.
- 2. Es una técnica destructiva que modifica la muestra.
- 3. Solamente puede emplearse en muestras líquidas.
- 4. Permite la preconcentración del analito sin uso de disolventes.
Explicación:
La Microextracción en Fase Sólida (SPME) es una técnica moderna de preparación de muestras que integra muestreo, extracción, concentración e introducción de la muestra en un solo paso.
- • Ventaja Principal: Libre de Disolventes (Opción 4):
- – Utiliza una fibra de sílice recubierta de una fase estacionaria polimérica (ej. polidimetilsiloxano).
- – Los analitos se adsorben o absorben directamente en la fibra hasta alcanzar el equilibrio.
- – Al acumularse en la fibra, los analitos se preconcentran significativamente. Posteriormente, la fibra se introduce directamente en el cromatógrafo (GC o HPLC) para la desorción térmica o con disolvente, eliminando la necesidad de usar disolventes orgánicos tóxicos durante la extracción. Es una técnica de «Química Verde».
- • Refutación de otras opciones:
- – Opción 2: Es no destructiva (especialmente en modo espacio de cabeza o «headspace»), ya que solo extrae una pequeña fracción del analito en equilibrio.
- – Opción 3: Es muy versátil; se usa para gases, líquidos y, mediante la técnica de espacio de cabeza (Headspace-SPME), para analizar volátiles en muestras sólidas sin tocarlas.
Pregunta 112
En cromatografía líquida, ¿qué condición se cumple en la cromatografía en fase reversa o inversa?:
- 1. Al aumentar la hidrofobicidad del analito aumenta su retención.
- 2. El componente menos polar eluye primero.
- 3. Las moléculas polares son retenidas más fuertemente que las no polares.
- 4. Las interacciones iónicas son fuertes.
Explicación:
La cromatografía en fase reversa (RP-HPLC) es la modalidad más utilizada en laboratorios farmacéuticos y bioquímicos. Su principio es justamente el «inverso» al histórico (fase normal).
- • El Sistema (Fases):
- – Fase Estacionaria: Es apolar (hidrofóbica). Generalmente sílice modificada con cadenas de hidrocarburos (ej. C18 u octadecisilano).
- – Fase Móvil: Es polar (ej. agua, metanol, acetonitrilo).
- • Mecanismo de Retención:
- – Se basa en interacciones hidrofóbicas (fuerzas de Van der Waals). «Lo semejante retiene a lo semejante».
- – Analitos Polares: Prefieren la fase móvil (agua). No interactúan con la fase estacionaria grasa y eluyen primero (tiempos de retención cortos).
- – Analitos Apolares (Hidrofóbicos): Tienen gran afinidad por las cadenas C18 de la columna. Se «pegan» a ella y se retrasan. Por tanto, cuanto más hidrofóbica es la molécula, mayor es su retención.
Pregunta 113
En la espectrometría de masas con plasma de acoplamiento inductivo (ICP-MS), ¿en la cuantificación de qué isótopo afecta la presencia de la interferencia poliatómica ArO+?:
- 1. 52Cr+.
- 2. 56Fe+.
- 3. 63Cu+.
- 4. 75As+.
Explicación:
En ICP-MS, las interferencias poliatómicas se producen cuando iones del gas del plasma (Argón) se combinan con iones de la matriz o del disolvente (Oxígeno del agua, Nitrógeno del aire, etc.) formando especies moleculares cargadas que tienen la misma masa que el analito.
- • Cálculo de la masa de la interferencia (ArO+):
- – El isótopo más abundante del Argón es 40Ar (~99.6%).
- – El isótopo más abundante del Oxígeno es 16O (~99.7%).
- – La suma de sus masas es: 40 + 16 = 56 u.
- • Solapamiento con el analito:
- – El isótopo más abundante del Hierro es el 56Fe (91.7%).
- – Debido a que el espectrómetro de masas cuadrupolar estándar no tiene resolución suficiente para distinguir 55.9349 u (Fe) de 55.9573 u (ArO), la señal del ArO+ se suma a la del hierro, falseando el resultado.
- – Este es el problema clásico del análisis de hierro por ICP-MS, que requiere celdas de colisión/reacción (KED) o espectrometría de alta resolución para resolverse.
- • Otras interferencias comunes (para descartar):
- – 75As+: Sufre interferencia de ArCl+ (40 + 35 = 75).
- – 52Cr+: Sufre interferencia de ArC+ (40 + 12 = 52).
Pregunta 114
¿Cuál de las siguientes características favorece que una molécula sea adecuada para su análisis mediante una fuente de ionización por electrospray (ESI)?:
- 1. Alta volatilidad y baja polaridad.
- 2. Alta polaridad y capacidad para formar iones en solución.
- 3. Peso molecular muy bajo y naturaleza apolar.
- 4. Insolubilidad en disolventes polares.
Explicación:
La ionización por electrospray (ESI) es una técnica de «ionización suave» que permite analizar moléculas grandes, no volátiles y térmicamente lábiles, transfiriendo iones preexistentes desde la fase líquida a la fase gaseosa.
- • Requisitos del Analito (Opción 2):
- – Polaridad: Las moléculas deben ser polares para disolverse en los disolventes compatibles con ESI (agua, metanol, acetonitrilo) y para interactuar con el campo eléctrico.
- – Ionización en solución: El mecanismo de ESI se basa en la desolvatación de gotas cargadas. Por tanto, el analito debe existir como ion en la disolución (ya sea protonado [M+H]+ o desprotonado [M-H]–) antes o durante el proceso de nebulización.
- • Comparación con otras técnicas:
- – Las características de alta volatilidad, baja polaridad y bajo peso molecular (opciones 1 y 3) son ideales para la Ionización por Impacto Electrónico (EI) usada en Cromatografía de Gases (GC-MS), no para LC-MS con ESI.
- – La insolubilidad en disolventes polares (opción 4) haría imposible preparar la muestra para ESI, ya que requiere un medio conductor líquido.
Pregunta 115
Un procedimiento analítico tiene un límite de detección de 0,02 mg/L, un límite de cuantificación de 0,2 mg/L y la respuesta es lineal en un intervalo hasta 10 mg/L. ¿Qué concentración de analito podría determinarse con exactitud?:
- 1. 0,1 mg/L.
- 2. 12 mg/L.
- 3. 4 mg/L.
- 4. 0,05 mg/L.
Explicación:
Para que una concentración pueda determinarse con exactitud y precisión aceptables (análisis cuantitativo), debe encontrarse dentro del Intervalo Dinámico Lineal del método.
- • Definición del Rango Útil:
- – Límite Inferior: Viene dado por el Límite de Cuantificación (LOQ). Por debajo de este valor (entre LOD y LOQ), se detecta la presencia del analito, pero el error es demasiado alto para dar un valor exacto. En este caso: LOQ = 0,2 mg/L.
- – Límite Superior: Viene dado por el Límite de Linealidad (LOL). Por encima de este valor, la respuesta deja de ser proporcional y el cálculo directo es erróneo. En este caso: LOL = 10 mg/L.
- – Conclusión: Solo podemos cuantificar valores en el intervalo [0,2 mg/L — 10 mg/L].
- • Evaluación de las opciones:
- – Opción 1 (0,1 mg/L) y Opción 4 (0,05 mg/L): Ambos son valores > LOD (0,02) pero < LOQ (0,2). Se detectan, pero no se cuantifican con exactitud.
- – Opción 2 (12 mg/L): Es > 10 mg/L. Está fuera del rango lineal. Se requeriría dilución para medirlo con exactitud.
- – Opción 3 (4 mg/L): Es el único valor que cae dentro del rango [0,2 – 10].
Pregunta 116
La permanganimetría es una de las técnicas utilizadas en el análisis cuantitativo en química. Indique cuál de las siguientes afirmaciones es VERDADERA:
- 1. Es necesario añadir un indicador de oxidación reducción.
- 2. Para realizarla en medio ácido, es necesario añadir un ácido oxidable por el permanganato de potasio.
- 3. Es necesario calentar porque la reacción es inicialmente muy rápida.
- 4. Es necesario estandarizar el permanganato de potasio porque no reúne los requisitos de un patrón primario.
Explicación:
El permanganato de potasio (KMnO4) es un oxidante fuerte muy utilizado, pero presenta características específicas que definen su manejo en el laboratorio.
- • ¿Por qué es cierta la Opción 4? (No es patrón primario):
- – El KMnO4 sólido rara vez se obtiene con una pureza del 100%. Suele estar contaminado con dióxido de manganeso (MnO2).
- – Además, en disolución acuosa es inestable; reacciona con la materia orgánica del agua, el polvo o la luz, descomponiéndose.
- – Por ello, sus disoluciones deben prepararse, hervirse, filtrarse y, obligatoriamente, estandarizarse frente a un patrón primario como el oxalato de sodio (Na2C2O4).
- • Análisis de las opciones falsas:
- – Opción 1: Falso. El permanganato actúa como autoindicador. Su color violeta intenso desaparece al reducirse a Mn2+ (incoloro). El punto final lo marca la aparición de un color rosa pálido persistente por el primer exceso de permanganato.
- – Opción 2: Falso. Se debe usar un ácido que NO reaccione con el permanganato (como H2SO4). Si usamos HCl, el permanganato oxidaría el cloruro a cloro gas (Cl2), cometiendo un error grave.
- – Opción 3: Falso. Se calienta (ej. con oxalato) porque la reacción es inicialmente muy lenta. Una vez formada una pequeña cantidad de producto (Mn2+), este actúa como catalizador (autocatalisis) y acelera la reacción.
Pregunta 117
El procedimiento general para la identificación de una sustancia por el método clásico de análisis cualitativo consiste en:
- 1. Provocar en la misma un cambio en sus propiedades que sea fácilmente observable y que se corresponda con la constitución de dicha sustancia.
- 2. Monitorizar un cambio espontáneo en la sustancia para determinar su naturaleza.
- 3. Provocar en la misma una degradación parcial para medir su concentración.
- 4. Medir sus propiedades fisicoquímicas para lograr la determinación.
Explicación:
El Análisis Cualitativo Clásico (o «Química Húmeda») se basa en la reactividad química para identificar los componentes de una muestra («¿Qué es?»).
- • Fundamento (Opción 1):
- – El analista añade un reactivo específico a la muestra para provocar una reacción química.
- – Esta reacción debe generar un producto con propiedades nuevas y fácilmente observables por los sentidos humanos, como:
- Aparición de un precipitado (cambio de estado).
- Cambio de color característico.
- Desprendimiento de un gas (burbujeo u olor).
- – Ejemplo: Añadir ión plata (Ag+) a una muestra con cloruros (Cl–) provoca la aparición inmediata de un sólido blanco (AgCl).
- • Descarte de otras opciones:
- – Opción 2: Rara vez se espera a un cambio «espontáneo»; el análisis requiere intervención activa.
- – Opción 3: Habla de medir «concentración», lo cual define al análisis cuantitativo, no cualitativo.
- – Opción 4: Medir propiedades fisicoquímicas (como punto de fusión o índice de refracción) es válido para la identificación, pero la definición «clásica» por excelencia se refiere a las reacciones químicas de la marcha analítica descritas en la opción 1.
Pregunta 118
¿Qué núcleos son activos y por lo tanto detectables mediante la técnica de resonancia magnética nuclear?:
- 1. 1H, 13C, 19F, 31P.
- 2. 1H, 12C, 19F, 31P.
- 3. 1H, 14C, 16O, 31P.
- 4. 1H, 14C, 16O, 19F.
Explicación:
Para que un núcleo atómico pueda absorber radiación electromagnética en la región de radiofrecuencias bajo un campo magnético (es decir, ser activo en RMN), debe poseer un momento magnético neto, lo cual requiere que su número cuántico de espín nuclear (I) sea distinto de cero.
- • Reglas de Selección:
- – Activos (Espín ½): Núcleos con número másico impar. Son los más fáciles de estudiar. Ejemplos: 1H, 13C, 19F, 31P.
- – Activos (Espín entero > 0): Núcleos con masa par y número atómico impar (Z). Ejemplos: 2H, 14N.
- – Inactivos (Espín = 0): Núcleos con número másico par y número atómico par (Par-Par). Estos núcleos no tienen momento magnético y son invisibles a la RMN. Los ejemplos más importantes son el 12C y el 16O.
- • Análisis de las opciones:
- – Opción 2: Incorrecta porque incluye 12C (inactivo).
- – Opciones 3 y 4: Incorrectas porque incluyen 16O (inactivo).
- – Opción 1: Todos los isótopos listados tienen número másico impar y espín ½, siendo los núcleos más utilizados en espectroscopía RMN.
Pregunta 119
¿Cuál es la afirmación VERDADERA en cuanto a la técnica de separación cromatográfica?:
- 1. Fases móviles comunes son el gel de sílice y la alúmina.
- 2. Los analitos que presentan una mayor interacción con la fase estacionaria permanecen menos tiempo en la columna de separación.
- 3. Un disolvente polar tendrá una mayor fuerza de elución que uno no polar en cromatografía de placa fina.
- 4. La cromatografía no permite separar compuestos mezclados en una disolución.
Explicación:
Analicemos los conceptos básicos de la cromatografía, específicamente en capa fina (TLC), que usualmente opera en «fase normal».
- • Análisis de la Opción 3 (Verdadera):
- – En TLC convencional, la fase estacionaria es polar (ej. sílice o alúmina). Los analitos polares se quedan «pegados» a ella.
- – Para desplazarlos (eluir), necesitamos un disolvente que compita por los sitios activos de la sílice.
- – Un disolvente polar tiene mayor capacidad para disolver los analitos polares y desplazar a los competidores de la fase estacionaria. Por tanto, en la serie eluotrópica, la polaridad equivale a fuerza de elución (hace que los compuestos «corran» más y tengan mayor Rf).
- • Errores en las otras opciones:
- – Opción 1: Gel de sílice y alúmina son sólidos, por lo que funcionan como Fases Estacionarias, no móviles.
- – Opción 2: Es al revés. Si un analito interactúa mucho con la fase estacionaria, se retrasa y su tiempo de retención aumenta.
- – Opción 4: Falso por definición; la cromatografía es, precisamente, una técnica de separación.
Pregunta 120
¿Qué referencia se utiliza para calcular la exactitud de un método analítico?:
- 1. Un falso positivo.
- 2. La media aritmética de un conjunto de resultados.
- 3. Un falso negativo.
- 4. El valor considerado como verdadero.
Explicación:
En la validación de métodos, es fundamental distinguir entre precisión y exactitud.
- • Definición de Exactitud (Opción 4):
- – La exactitud (o veracidad) mide el grado de concordancia entre el resultado de una medición (o la media de varias) y el valor verdadero (o valor de referencia aceptado) del analito en la muestra.
- – Se cuantifica mediante el cálculo del error absoluto (Valor Medido – Valor Verdadero) o el error relativo. Sin un «valor verdadero» conocido (proporcionado por un Material de Referencia Certificado), no se puede determinar la exactitud.
- • Descarte de otras opciones:
- – Opción 2 (Media): La media por sí sola solo nos da una medida de tendencia central. La dispersión alrededor de la media define la precisión, no la exactitud.
- – Opciones 1 y 3: Los falsos positivos/negativos son parámetros de rendimiento cualitativo (diagnóstico), relacionados con la especificidad y sensibilidad, no con la exactitud numérica.
Pregunta 121
¿Qué técnica es la más adecuada para medir la concentración en suero de las vitaminas liposolubles A y E?:
- 1. Cromatografía de gases.
- 2. Cromatografía líquida de alta eficacia (HPLC).
- 3. Espectroscopia de infrarrojo.
- 4. Potenciometría.
Explicación:
El análisis clínico de vitaminas en matrices biológicas complejas (como el suero) requiere una técnica que combine alta capacidad de separación con sensibilidad y condiciones suaves.
- • ¿Por qué HPLC (Opción 2)?
- – Las vitaminas A (retinol) y E (tocoferol) son moléculas orgánicas grandes y, lo más importante, termolábiles (se degradan con el calor) y sensibles a la oxidación.
- – La HPLC permite trabajar a temperatura ambiente, evitando la descomposición térmica. Además, los detectores UV-Vis o de fluorescencia acoplados al HPLC son muy sensibles y selectivos para estas vitaminas. Es el «Gold Standard» en laboratorios clínicos.
- • Descarte de otras opciones:
- – Cromatografía de Gases (GC): Requiere vaporizar la muestra a altas temperaturas. Esto degradaría las vitaminas a menos que se realice una derivatización previa (proceso complejo y propenso a errores).
- – Infrarrojo (IR): Es una técnica de identificación cualitativa, no tiene la sensibilidad ni la capacidad de separación necesarias para cuantificar trazas en una mezcla compleja como el suero.
- – Potenciometría: Mide iones, no moléculas orgánicas complejas.
Pregunta 122
En la cromatografía de intercambio iónico, como por ejemplo para la separación de los iones lantánidos, ¿cómo afecta la interacción eluyente-soluto a la separación?:
- 1. A mayor interacción, mayor retención.
- 2. No influye, depende de otros factores.
- 3. A mayor interacción, elución más rápida.
- 4. A menor interacción, elución más rápida.
Explicación:
Para separar lantánidos (que tienen propiedades químicas y cargas muy similares, habitualmente +3), se utiliza cromatografía de intercambio iónico con un agente complejante en el eluyente (fase móvil), como el citrato o el ácido α-hidroxiisobutírico.
- • El mecanismo de competencia:
- – El ión metálico (soluto) se siente atraído por dos fuerzas opuestas: 1. La resina (Fase Estacionaria) → Lo retiene (frena). 2. El ligando en el eluyente (Fase Móvil) → Lo arrastra (acelera).
- • Interpretación de la interacción Eluyente-Soluto (Opción 3):
- – Si el soluto tiene una fuerte interacción con el eluyente, significa que forma un complejo soluble muy estable en la fase móvil.
- – Al estar fuertemente «agarrado» por el eluyente, el ión pasa menos tiempo pegado a la resina.
- – Resultado: El metal viaja más rápido a través de la columna. Por tanto, a mayor afinidad por el eluyente, menor tiempo de retención (elución más rápida).
- • Caso Lantánidos:
- – Los lantánidos más pesados (radio iónico menor) forman complejos más fuertes con el citrato (eluyente). Por eso, los lantánidos pesados eluyen primero y los ligeros al final.
Pregunta 123
¿Cuál es el pH en el equilibrio para una valoración entre ácido fluorhídrico e hidróxido sódico?:
- 1. 7, ambos son fuertes.
- 2. < 7, el ácido fluorhídrico es un ácido fuerte.
- 3. No se puede realizar la valoración, ambos son débiles.
- 4. > 7, el ácido fluorhídrico es un ácido débil.
Explicación:
El resultado del pH en el punto de equivalencia depende de la fuerza relativa del ácido y la base que reaccionan.
- 1. Naturaleza de los Reactivos:
- – NaOH (Hidróxido de sodio): Base fuerte (se disocia totalmente).
- – HF (Ácido fluorhídrico): Ácido débil. (A diferencia del HCl, HBr y HI, el enlace H-F es muy fuerte, lo que impide su disociación completa en agua).
- 2. Reacción de Neutralización: HF + NaOH → NaF + H2O En el punto de equivalencia, tenemos una disolución de fluoruro de sodio (NaF).
- 3. Hidrólisis de la Sal:
- – El catión Na+ no sufre hidrólisis (proviene de base fuerte).
- – El anión fluoruro (F–) es la base conjugada de un ácido débil, por lo que reacciona con el agua:
- F– + H2O ↔ HF + OH–
- – La generación de iones hidroxilo (OH–) hace que la disolución final sea básica (pH > 7).
Pregunta 124
Para el análisis de una muestra metálica se empieza con la disolución de ésta mediante agua regia. ¿Cuál de los siguientes metales NO se disolverá?:
- 1. Oro.
- 2. Platino.
- 3. Osmio.
- 4. Paladio.
Explicación:
El agua regia es una mezcla de HCl concentrado y HNO3 concentrado (proporción 3:1), famosa por disolver metales nobles mediante oxidación y formación de complejos clorados.
- • Metales Solubles:
- – Oro (Au): Se disuelve formando ácido cloroáurico (HAuCl4).
- – Platino (Pt): Se disuelve formando ácido cloroplatínico (H2PtCl6).
- – Paladio (Pd): Es el menos noble del grupo del platino; se disuelve fácilmente en agua regia e incluso en ácido nítrico caliente.
- • La Excepción (Osmio):
- – El Osmio (Os), junto con el Iridio (Ir), el Rutenio (Ru) y el Rodio (Rh), pertenece a los «metales del grupo del platino» que presentan una inercia química extrema en su forma metálica compacta.
- – El osmio compacto no es atacado por el agua regia. Para disolverlo, se requieren métodos más agresivos, como la fusión alcalina oxidante (con peróxido de sodio o hidróxido de sodio y nitrato).
Pregunta 125
En cromatografía de gases ¿cuál de los siguientes detectores NO se utiliza?:
- 1. Conductividad térmica.
- 2. Ionización de llama.
- 3. Captura electrónica.
- 4. Fluorescencia.
Explicación:
Los detectores en cromatografía de gases (GC) deben ser capaces de medir propiedades físicas o químicas de sustancias en estado gaseoso o de vapor a altas temperaturas.
- • Detectores Típicos de GC (Opciones 1, 2 y 3):
- – Conductividad Térmica (TCD): Universal. Mide cambios en la conducción de calor del gas portador.
- – Ionización de Llama (FID): Muy común para compuestos orgánicos. Quema la muestra y mide la corriente iónica.
- – Captura Electrónica (ECD): Específico para halógenos y compuestos electronegativos.
- • La Excepción (Opción 4):
- – La Fluorescencia es el detector por excelencia en Cromatografía Líquida (HPLC).
- – Aunque existen aplicaciones muy específicas de fluorescencia atómica en gases, no es un detector estándar para GC molecular debido a la dificultad de excitar moléculas en fase gas sin descomponerlas y a los problemas de «quenching» (desactivación de la fluorescencia) por colisiones en el gas.
Pregunta 126
¿Cuál es la opción VERDADERA con relación a la absorción atómica de un elemento?:
- 1. Las interferencias químicas se pueden evitar usando el método de adiciones estándar.
- 2. En absorción atómica con llama se pueden producir interferencias espectrales por la presencia de productos de combustión.
- 3. Se pueden utilizar agentes complejantes para minimizar el efecto de las interferencias espectrales.
- 4. No existe ningún método para corregir la absorción debida al fondo.
Explicación:
La Espectroscopía de Absorción Atómica (AAS) está sujeta a diversas interferencias que deben conocerse para validar la técnica.
- • Análisis de la Opción 2 (Verdadera):
- – La llama no es un medio perfectamente transparente. La combustión del combustible y el oxidante genera especies moleculares y radicales (como OH, CN, C2) que absorben radiación en bandas anchas.
- – Esta absorción de fondo por la propia llama constituye una interferencia espectral, ya que se superpone a la señal del analito.
- • Refutación de las otras opciones:
- – Opción 1: El método de adiciones estándar corrige efectos de matriz (viscosidad, transporte), pero NO elimina interferencias químicas específicas como la formación de óxidos refractarios (para eso se usan «agentes liberadores» o llamas más calientes).
- – Opción 3: Los agentes complejantes (como el EDTA) se usan para evitar interferencias químicas (mejorar la atomización), no espectrales.
- – Opción 4: Falso. Existen varios métodos eficaces para corregir el fondo, como la lámpara de deuterio, el efecto Zeeman o el método Smith-Hieftje.
Pregunta 127
El intervalo de viraje del indicador ácido-base naranja de metilo es 3,1-4,4. Señale la respuesta correcta:
- 1. Es un indicador adecuado para la detección visual del punto final de la valoración de un ácido fuerte con una base fuerte.
- 2. El indicador cambia de color cuando el pH de la disolución en la que está disuelto es menor que pH 3,1.
- 3. No es un indicador adecuado para la valoración de un ácido fuerte con una base fuerte.
- 4. El indicador cambia de color cuando el pH de la disolución en la que está disuelto es mayor que pH 4,4.
Explicación:
Para seleccionar el indicador correcto en una volumetría ácido-base, debemos comparar el intervalo de transición del indicador con el pH del punto de equivalencia de la reacción.
- • El Criterio de Selección (Opción 3 – Correcta):
- – En la valoración de un Ácido Fuerte con una Base Fuerte (ej. HCl con NaOH), el punto de equivalencia se sitúa exactamente a pH 7 (neutro).
- – Un indicador se considera «adecuado» teóricamente si su intervalo de viraje incluye el pH del punto de equivalencia.
- – El naranja de metilo vira entre 3,1 y 4,4. Como el pH 7 queda fuera de este rango, el indicador cambiará de color mucho antes (o después) de alcanzar la neutralidad real, introduciendo un error de valoración. Lo ideal sería usar azul de bromotimol (6,0-7,6) o fenolftaleína (8,0-10,0).
- • Análisis de las otras opciones:
- – Opción 1: Aunque se usa en prácticas docentes porque el salto de pH es muy vertical, en rigor analítico no es el más adecuado debido al error sistemático que introduce respecto al pH 7.
- – Opciones 2 y 4: Son conceptualmente erróneas. El indicador «cambia» DENTRO del intervalo. Por debajo de 3,1 ya TIENE su color ácido (rojo) y por encima de 4,4 ya TIENE su color básico (amarillo). No cambia fuera de esos límites.
Pregunta 128
Acerca del método de calibración del estándar interno señale la respuesta VERDADERA:
- 1. La señal de respuesta es la relación entre la señal del analito y la del estándar interno.
- 2. Se representa la relación entre la respuesta del analito y la del estándar interno frente a la concentración de estándar interno.
- 3. Se adiciona una cantidad conocida del estándar interno sólo a las muestras.
- 4. El estándar interno elegido como especie de referencia no debe ser similar al analito.
Explicación:
El método del estándar interno (IS) se utiliza para corregir errores aleatorios y sistemáticos en el análisis instrumental (como variaciones en el volumen de inyección o deriva del detector).
- • Fundamento (Opción 1 – Correcta):
- – Se añade una cantidad fija y conocida de una sustancia diferente (el Estándar Interno) a todas las soluciones (blancos, calibradores y muestras).
- – Para cuantificar, no se usa la señal absoluta del analito, sino la relación de señales:Respuesta = (Señal Analito) / (Señal Estándar Interno).
- – Si hay una pérdida de muestra o un fallo instrumental, ambas señales disminuirán proporcionalmente, pero su cociente se mantendrá constante, corrigiendo el error.
- • Errores en las otras opciones:
- – Opción 2: En el eje X se representa la concentración del analito (que es la variable), no la del estándar interno (que es constante).
- – Opción 3: Debe añadirse a TODAS las soluciones (patrones y muestras) para que la comparación sea válida.
- – Opción 4: El IS debe ser lo más similar posible al analito (física y químicamente) para comportarse igual durante el proceso, pero diferenciable analíticamente (ej. deuterado en masas o con diferente tiempo de retención).
Pregunta 129
¿Cuál es la respuesta FALSA respecto a los parámetros de calidad de los métodos analíticos?:
- 1. La sensibilidad de calibración es la ordenada en el origen de la curva de calibrado.
- 2. La sensibilidad analítica es la relación entre la pendiente de la curva de calibrado respecto a la desviación estándar de la señal analítica a una determinada concentración de analito.
- 3. El límite de detección es la concentración más pequeña que se puede detectar con un cierto nivel de confianza.
- 4. El intervalo dinámico lineal de un método analítico se refiere al intervalo de concentración en el que se puede realizar la determinación con una curva de calibrado lineal.
Explicación:
Para identificar la afirmación falsa, debemos repasar la definición matemática de la recta de calibrado y sus parámetros de desempeño según la IUPAC.
- • Análisis de la Opción 1 (La Falsa):
- – La ecuación de una recta de calibrado es: Señal = m·Concentración + b.
- – La ordenada en el origen (b) representa la señal instrumental del blanco (cuando la concentración es cero), no la sensibilidad.
- – La sensibilidad de calibración se define como la capacidad del método para diferenciar pequeñas variaciones de concentración. Matemáticamente, corresponde a la pendiente (m) de la curva. A mayor pendiente, mayor sensibilidad.
- • Veracidad de las otras opciones:
- – Opción 2: Correcta. La sensibilidad analítica (γ) incorpora la precisión: γ = m / ss (donde ss es la desviación estándar de la señal). Es un parámetro más robusto que la pendiente sola porque penaliza a los métodos con mucho ruido instrumental.
- – Opción 3: Definición correcta de LOD (Límite de Detección).
- – Opción 4: Definición correcta del rango lineal.
Pregunta 130
Respecto a los métodos gravimétricos de análisis señale la respuesta VERDADERA:
- 1. Si es necesario, el precipitado se transforma en un producto de composición desconocida mediante el tratamiento térmico adecuado.
- 2. El precipitado obtenido debe tener una solubilidad lo suficientemente alta para que no haya pérdidas durante la filtración y el lavado.
- 3. La solubilidad del precipitado, la temperatura, la concentración de los reactivos y la velocidad con la que se mezclan influyen en el tamaño de partícula del precipitado.
- 4. Durante la formación del precipitado, si el mecanismo predominante es la nucleación se obtendrá un precipitado que contiene muchas partículas de gran tamaño.
Explicación:
El éxito de una gravimetría depende de obtener un precipitado puro y fácil de filtrar (cristales grandes). Esto se explica mediante la teoría de la sobresaturación relativa de Von Weimarn.
- • Factores que influyen (Opción 3 – Verdadera):
- – El tamaño de partícula depende de la relación: (Q – S) / S, donde Q es la concentración de reactivos y S es la solubilidad.
- – Para obtener cristales grandes (fáciles de filtrar), queremos que este valor sea bajo.
- – Por tanto, controlamos la temperatura (aumenta S), la concentración (mantiene Q bajo) y la velocidad de mezcla (evita zonas de Q muy alto) para favorecer el crecimiento cristalino. Todos estos factores son determinantes.
- • Errores en las otras opciones:
- – Opción 1: El producto final debe ser de composición conocida y constante para poder hacer los cálculos estequiométricos.
- – Opción 2: La solubilidad debe ser baja (despreciable) para que el analito no se pierda al lavar el precipitado.
- – Opción 4: Si predomina la nucleación, se forman millones de núcleos diminutos simultáneamente, resultando en un precipitado coloidal (partículas muy pequeñas), no grande.
Pregunta 131
¿Por qué se caracterizan las disoluciones de nitrato de plata?:
- 1. No son disoluciones patrón.
- 2. Se utilizan para determinar las concentraciones de iones haluros en disoluciones acuosas.
- 3. Se utilizan para obtener curvas de valoración por formación de complejos.
- 4. Su concentración no influye en el cambio de pAg en el punto de equivalencia de una curva de valoración por precipitación.
Explicación:
El nitrato de plata (AgNO3) es el reactivo valorante más importante en las volumetrías de precipitación, conjunto de técnicas conocidas genéricamente como Argentometría.
- • Aplicación Principal (Opción 2):
- – La reacción fundamental es la formación de sales de plata insolubles:
- Ag+ (ac) + X– (ac) → AgX (s) ↓
- – Esta reacción es cuantitativa, rápida y estequiométrica para los haluros (Cloruros Cl–, Bromuros Br–, Yoduros I–) y pseudohaluros (como Tiocianato SCN–), permitiendo su determinación exacta mediante métodos clásicos como Mohr, Volhard o Fajans.
- • Análisis de las opciones falsas:
- – Opción 1: Falso. El AgNO3 de alta pureza puede usarse como patrón primario. Si no es lo suficientemente puro, se estandariza frente a NaCl (patrón primario), convirtiéndose en disolución patrón.
- – Opción 3: Aunque la plata puede formar complejos (ej. con cianuro), su uso «característico» y masivo en el laboratorio analítico es la precipitación, no la complexometría (donde domina el EDTA).
- – Opción 4: Falso. Como en toda valoración, cuanto mayor sea la concentración de los reactivos, mayor es el salto (la magnitud del cambio de pAg) en la zona de equivalencia, facilitando la detección del punto final.
Pregunta 132
Con relación a la teoría de orbitales moleculares para una molécula dinuclear, indique la respuesta VERDADERA:
- 1. Un orbital molecular con simetría cilíndrica alrededor del eje internuclear se llama orbital pi.
- 2. Los electrones de la molécula no pertenecen a enlaces particulares, sino que están repartidos por la molécula.
- 3. En un orbital molecular enlazante el solapamiento electrónico en el eje internuclear es destructivo.
- 4. El orden de enlace es igual a la semisuma de los electrones enlazantes más los electrones antienlazantes.
Explicación:
La Teoría de Orbitales Moleculares (TOM) supone un cambio de paradigma respecto a la Teoría de Enlace de Valencia (TEV).
- • Deslocalización Electrónica (Opción 2 – Verdadera):
- – En la TOM, los electrones no están confinados en un enlace localizado entre dos átomos (como los puntos en una estructura de Lewis).
- – Se considera que los electrones ocupan orbitales moleculares que se extienden sobre toda la molécula (son policéntricos). Incluso en una molécula dinuclear, el orbital pertenece al conjunto de los dos núcleos, no a uno solo.
- • Corrección de las otras opciones:
- – Opción 1: La simetría cilíndrica (rotación sin cambio de fase) define a los orbitales sigma (σ). Los orbitales pi (π) tienen un plano nodal que contiene al eje internuclear.
- – Opción 3: El solapamiento destructivo (resta de funciones de onda) genera orbitales antienlazantes (con mayor energía y nodos). Los enlazantes provienen de interferencia constructiva (suma).
- – Opción 4: El orden de enlace se calcula restando, no sumando: OE = (Nº e– enlazantes – Nº e– antienlazantes) / 2.
Pregunta 133
Indique cuál de las siguientes afirmaciones, relativas al primer principio de la Termodinámica, es FALSA:
- 1. El primer principio establece que la energía de un sistema cerrado se conserva.
- 2. Para una transformación cíclica de cualquier sistema la variación de energía interna es nula.
- 3. La variación de una función de estado asociada a un proceso reversible o irreversible es la misma si los estados inicial y final son los mismos por las dos vías.
- 4. Calor y trabajo no son equivalentes.
Explicación:
El Primer Principio de la Termodinámica es, esencialmente, la ley de conservación de la energía, pero hay que tener cuidado con el «dónde» se conserva.
- • Análisis de la Opción 1 (Falsa):
- – Un sistema cerrado es aquel que puede intercambiar energía (calor y trabajo) con su entorno, aunque no intercambie materia.
- – La formulación matemática es: ΔU = Q + W. Si el sistema recibe calor o trabajo, su energía interna (U) aumenta; si los cede, disminuye. Por tanto, su energía no es constante (no se conserva dentro del sistema).
- – Lo que se conserva es la energía del Universo (Sistema + Entorno), que equivale a un sistema aislado.
- • Veracidad de las otras opciones:
- – Opción 2 y 3: La energía interna (U) es una función de estado. Su valor depende solo del estado actual, no del camino recorrido. En un ciclo (inicio = final), la variación es cero.
- – Opción 4: Aunque Joule demostró el «equivalente mecánico del calor», termodinámicamente no son idénticos: el trabajo puede transformarse íntegramente en calor, pero el calor no puede transformarse íntegramente en trabajo (limitación del Segundo Principio).
Pregunta 134
Con relación a la presión osmótica, indique la afirmación VERDADERA:
- 1. Para que se dé este fenómeno se necesita una membrana semipermeable entre disoluciones de diferente concentración, la cual deja pasar moléculas de soluto, pero no de disolvente.
- 2. Entre dos disoluciones no isotónicas el efecto de presión osmótica es nulo.
- 3. Cuando tenemos solutos electrolíticos, la expresión de la presión osmótica se corrige con el factor de Van’t Hoff.
- 4. La disolución pasa siempre al medio más diluido.
Explicación:
La presión osmótica (π) es una propiedad coligativa, lo que significa que depende exclusivamente del número de partículas disueltas, y no de su naturaleza química.
- • El Factor de Van’t Hoff (Opción 3 – Verdadera):
- – La ecuación básica es: π = M·R·T.
- – Sin embargo, si el soluto es un electrolito (ej. NaCl), se disocia en iones. 1 mol de NaCl genera 2 moles de partículas (Na+ y Cl–).
- – Como la presión osmótica «cuenta» partículas, la ecuación debe corregirse multiplicando por el factor i (factor de Van’t Hoff), quedando: π = i·M·R·T.
- • Errores en las otras opciones:
- – Opción 1: La definición es justo al revés. Una membrana semipermeable deja pasar el disolvente (moléculas pequeñas como agua) y retiene el soluto.
- – Opción 2: Si no son isotónicas (tienen diferente concentración), existe un gradiente de presión osmótica y habrá flujo neto.
- – Opción 4: El flujo espontáneo del disolvente va desde la disolución más diluida (menos soluto) hacia la más concentrada, intentando igualar las concentraciones.
Pregunta 135
Señale, de las siguientes afirmaciones sobre el coeficiente de difusión de una especie química, cuál es VERDADERA:
- 1. La ecuación de Stokes-Einstein establece que el coeficiente de difusión es inversamente proporcional a la viscosidad del medio, y proporcional tanto al tamaño de la partícula como a la temperatura.
- 2. La segunda ley de Fick establece que el flujo de materia por difusión y el gradiente de materia son proporcionales.
- 3. Tiene dimensiones de distancia al cuadrado dividido por tiempo.
- 4. El desplazamiento aleatorio de una especie por difusión se caracteriza por la distancia cuadrática media, la cual aumenta con el tiempo independientemente del valor del coeficiente de difusión.
Explicación:
El coeficiente de difusión (D) es el parámetro cinético que cuantifica la facilidad con la que una partícula se mueve en un medio debido a la energía térmica.
- • Análisis Dimensional (Opción 3 – Verdadera):
- – Según la 1ª Ley de Fick: Flujo (J) = -D · (gradiente de concentración).
- – Las unidades de flujo son mol·m-2·s-1.
- – Las unidades de gradiente son (mol·m-3) / m = mol·m-4.
- – Despejando D: (mol·m-2·s-1) / (mol·m-4) = m2·s-1. Esto corresponde a longitud al cuadrado dividido por tiempo.
- • Errores en las otras opciones:
- – Opción 1: La ecuación de Stokes-Einstein es D = kT / (6πηr). El coeficiente es inversamente proporcional al radio de la partícula (r), no proporcional. (Partículas más grandes difunden más lento).
- – Opción 2: Esa definición corresponde a la Primera Ley de Fick. La Segunda Ley relaciona la variación de concentración con el tiempo.
- – Opción 4: La distancia cuadrática media se define como <x2> = 2Dt. Por tanto, depende directamente del valor de D.
Pregunta 136
De las siguientes afirmaciones, relacionadas con los espectros electrónicos de una molécula, indique la VERDADERA:
- 1. Las transiciones singlete-singlete son procesos lentos, que pueden durar horas.
- 2. Las transiciones triplete-singlete cesan en cuanto desaparece la fuente de radiación.
- 3. Los procesos de fosforescencia y fluorescencia son ejemplos de transiciones no radiactivas.
- 4. Si se produce un cruce de sistemas, por ejemplo de un estado singlete a uno triplete, la molécula decae al estado fundamental mediante el proceso de fosforescencia.
Explicación:
Para entender la luminiscencia, debemos seguir el camino de la energía en el diagrama de Jablonski.
- • El Mecanismo de Fosforescencia (Opción 4 – Verdadera):
- – 1. La molécula absorbe luz y sube a un estado excitado Singlete (S1).
- – 2. Ocurre un Cruce Inter-Sistemas (ISC): La molécula cambia su espín y pasa a un estado excitado Triplete (T1), que es de menor energía que S1 pero de distinta multiplicidad.
- – 3. El regreso desde el Triplete (T1) al estado fundamental Singlete (S0) está «prohibido» por las reglas de selección de espín. Sin embargo, ocurre lentamente emitiendo un fotón. Esta emisión retardada es la fosforescencia.
- • Análisis de errores:
- – Opción 1: Las transiciones S-S (como la fluorescencia) son permitidas y muy rápidas (nanosegundos).
- – Opción 2: Al ser procesos prohibidos, la vida media del triplete es larga. La fosforescencia persiste un tiempo después de apagar la fuente (efecto «glow in the dark»).
- – Opción 3: Ambos procesos implican emisión de fotones (luz), por lo tanto son transiciones radiactivas. Lo «no radiactivo» sería la relajación vibracional o el cruce entre sistemas.
Pregunta 137
¿Qué afirma la ley de Hess?:
- 1. Que la entalpía depende del mecanismo de reacción.
- 2. Que la variación de entalpía de un proceso neto es la suma de las variaciones de entalpía de sus etapas constituyentes.
- 3. Que la entalpía no es función de estado.
- 4. Que la entalpía solo se aplica a combustiones.
Explicación:
La Ley de Hess (1840) es una consecuencia directa del Primer Principio de la Termodinámica y de la naturaleza de la entalpía.
- • Propiedad Fundamental: Función de Estado:
- – La entalpía (H) es una función de estado, lo que significa que su variación (ΔH) depende únicamente de los estados inicial (reactivos) y final (productos), y es independiente del camino o mecanismo seguido para ir de uno a otro.
- • Enunciado de la Ley (Opción 2 – Verdadera):
- – «Si una reacción química se puede expresar como la suma algebraica de una serie de reacciones intermedias, el calor de reacción total (ΔHtotal) es igual a la suma algebraica de los calores de las reacciones parciales».
- – Esto permite calcular entalpías de reacción difíciles de medir experimentalmente combinando datos conocidos (como entalpías de formación o de combustión).
Pregunta 138
Indique cuál de estas afirmaciones relativas a la técnica de difracción de rayos X es VERDADERA:
- 1. Los rayos X son un tipo de radiación electromagnética de baja energía, del orden de las distancias atómicas en sólidos.
- 2. Los rayos X interaccionan con los neutrones de cada átomo o ion que se encuentre dentro de la trayectoria del haz.
- 3. La técnica de difracción de rayos X permite obtener información a partir de la interferencia destructiva de los rayos dispersados.
- 4. La técnica de difracción de rayos X permite obtener información sobre la separación interatómica.
Explicación:
La cristalografía de rayos X es la técnica principal para determinar la estructura atómica y molecular de un cristal mediante la dispersión de un haz de rayos X.
- • Análisis de la Opción 4 (Verdadera):
- – Se basa en la Ley de Bragg: nλ = 2d·sen(θ).
- – Esta ley relaciona el ángulo de incidencia (θ) y la longitud de onda (λ) con la distancia entre planos atómicos (d).
- – Al medir los ángulos e intensidades de los rayos difractados, podemos calcular las distancias interatómicas y reconstruir la disposición tridimensional de los átomos (la celda unidad).
- • Errores en las otras opciones:
- – Opción 1: Los rayos X son de alta energía (alta frecuencia, longitud de onda corta). Su longitud de onda (0.1 – 10 nm) sí coincide con las distancias interatómicas, pero su energía es mucho mayor que la visible.
- – Opción 2: Los fotones de rayos X interactúan con la nube electrónica de los átomos, no con el núcleo (neutrones). La difracción de neutrones es otra técnica distinta.
- – Opción 3: Los patrones de difracción (picos o puntos brillantes) son resultado de la interferencia constructiva (cuando las ondas están en fase), no destructiva.
Pregunta 139
¿Qué técnicas de análisis NO se basan en las distintas radiaciones generadas al interaccionar rayos X con la materia?:
- 1. Técnicas de radiación de fluorescencia.
- 2. Técnicas de emisión de rayos X.
- 3. Técnicas basadas en el efecto fotoeléctrico.
- 4. Técnicas de difracción de rayos X.
Explicación:
La interacción de los rayos X con la materia puede dar lugar a dos tipos principales de fenómenos: absorción/emisión (inelásticos) y dispersión (elásticos).
- • Fenómenos de Generación/Emisión (Opciones 1, 2 y 3):
- – Fluorescencia (XRF): El átomo absorbe un rayo X, expulsa un electrón interno y, al relajarse, genera y emite un nuevo fotón de menor energía característico del elemento.
- – Efecto Fotoeléctrico (XPS): La interacción genera la emisión de un electrón (fotoelectrón).
- – En estos casos, hay transferencia de energía y se producen nuevas partículas o radiaciones secundarias.
- • Fenómeno de Dispersión Elástica (Opción 4 – Correcta):
- – La difracción de rayos X (XRD) se basa en la dispersión elástica (scattering de Thomson).
- – Los fotones incidentes chocan con los electrones y «rebotan» cambiando su dirección, pero conservando su energía original. No se genera nueva radiación ni cambia el estado energético del átomo.
- – Lo que medimos es la interferencia constructiva de esos mismos rayos incidentes desviados, no una emisión secundaria.
Pregunta 140
¿Qué dispositivo NO puede crear un campo magnético para la caracterización de materiales?:
- 1. Fuente de tensión continua regulada.
- 2. Imanes permanentes.
- 3. Bobinados resistivos con corriente eléctrica.
- 4. Electroimanes.
Explicación:
Para generar un campo magnético estático (magnetostático) se requiere, por definición física, el movimiento de cargas eléctricas (corriente) o momentos magnéticos intrínsecos alineados.
- • Generadores de Campo Magnético:
- – Imanes permanentes (Opción 2): Generan campo por el espín de sus electrones.
- – Electroimanes y Bobinados (Opciones 3 y 4): Al circular una corriente eléctrica por un conductor enrollado (solenoide), se induce un campo magnético en su interior (Ley de Ampère).
- • Análisis de la Opción 1 (La Falsa):
- – Una Fuente de Tensión Continua es un dispositivo que mantiene una diferencia de potencial eléctrico (Voltios).
- – Por sí sola, una fuente crea un campo eléctrico entre sus bornes, no magnético.
- – Solo si se conecta a una carga (como una bobina) fluirá corriente y la bobina generará el campo magnético, pero la fuente es solo el suministro de energía, no el elemento generador del campo magnético físico.
Pregunta 141
¿Qué diferencia hay entre un material con plasticidad y un material con elasticidad?:
- 1. En el tipo de deformación, si es longitudinal o transversal a la presión ejercida.
- 2. En la resistencia a la fuerza aplicada para mantenerse sin deterioro.
- 3. No hay ninguna diferencia, los conceptos son análogos.
- 4. El material con plasticidad no recupera su tamaño al cesar la presión ejercida y el material con elasticidad si lo hace.
Explicación:
En ciencia de materiales, la respuesta de un sólido ante una fuerza externa se describe mediante la curva esfuerzo-deformación.
- • Comportamiento Elástico (Reversible):
- – Ocurre cuando los átomos se desplazan ligeramente de sus posiciones de equilibrio sin romper enlaces.
- – Al cesar la fuerza, los átomos vuelven a su posición original.
- – Resultado: El material recupera totalmente su forma y tamaño inicial (como una goma elástica o un muelle).
- • Comportamiento Plástico (Irreversible):
- – Ocurre cuando se supera el límite elástico del material. Los planos atómicos se deslizan unos sobre otros (dislocaciones), rompiendo y reformando enlaces en nuevas posiciones.
- – Al retirar la fuerza, el material no regresa a su estado original.
- – Resultado: Queda una deformación permanente o residual (como al doblar un clip metálico o moldear plastilina).
Pregunta 142
El pH de una disolución neutra es igual a 7,00:
- 1. Independientemente de la temperatura/a cualquier temperatura.
- 2. Siempre que [H+] > [OH-].
- 3. Solo a 20 °C.
- 4. Solo a 25 °C.
Explicación:
La neutralidad de una disolución se define estrictamente cuando la concentración de protones es igual a la de hidroxilos: [H+] = [OH–]. El valor numérico del pH al que esto ocurre depende de la constante de autoionización del agua (Kw).
- • Dependencia de la Temperatura:
- – La reacción de autoionización (H2O ↔ H+ + OH–) es endotérmica.
- – Al aumentar la temperatura, el equilibrio se desplaza a la derecha, aumentando Kw.
- • Cálculos (Ejemplos):
- – A 25 °C: Kw = 1,0 × 10-14. Por tanto, [H+] = √Kw = 10-7. pH = 7,00.
- – A 60 °C: Kw aumenta a ~9,6 × 10-14. Entonces [H+] ≈ 3,1 × 10-7. pH ≈ 6,51. (A 60°C, el pH neutro es 6,51, no 7).
- – A 0 °C: Kw disminuye. El pH neutro es aproximadamente 7,47.
Pregunta 143
Las expresiones del descenso crioscópico, ΔTc = kc m2, y de la presión osmótica, Π = c2 RT son válidas:
- 1. Para cualquier disolución líquida.
- 2. Sólo para disoluciones líquidas ideales y diluidas.
- 3. Sólo para disoluciones líquidas ideales.
- 4. Sólo para disoluciones acuosas diluidas.
Explicación:
Estas fórmulas son lo que se conoce como Leyes Límites de las propiedades coligativas. Su derivación termodinámica implica dos suposiciones fundamentales:
- 1. Comportamiento Ideal:
- – Se asume que no existen fuerzas de interacción específicas entre soluto y disolvente que desvíen el comportamiento de la Ley de Raoult para el disolvente.
- 2. Condición de Dilución Infinita:
- – Matemáticamente, la derivación parte de la igualdad de potenciales químicos, donde aparece un término logarítmico: ln(xdisolvente).
- – Sabiendo que xdisolvente = 1 – xsoluto, se aplica la expansión en serie de Taylor: ln(1 – x) ≈ -x.
- – Esta aproximación matemática (que permite obtener una relación lineal simple como ΔT = k·m) solo es válida matemáticamente cuando la concentración de soluto (x) es muy pequeña (diluida).
- • Descarte de otras opciones:
- – Opción 1 y 3: En disoluciones concentradas (aunque fueran ideales), la aproximación lineal falla. En disoluciones reales, se requieren coeficientes de actividad.
- – Opción 4: Estas leyes son universales para cualquier disolvente (benceno, etanol, etc.), no solo agua, siempre que se use la constante (kc) específica de ese disolvente.
Pregunta 144
La reacción del óxido nítrico con hidrógeno a 1280 °C es 2NO (g) + 2H2 (g) → N2 (g) + 2H2O (g). A partir de los siguientes datos, medidos a dicha temperatura, ¿cuál es el orden global de la reacción?:
| Experimento | [NO] (M) | [H2] (M) | Velocidad inicial (M/s) |
|---|---|---|---|
| 1 | 5,0 × 10-3 | 2,0 × 10-3 | 1,3 × 10-5 |
| 2 | 10,0 × 10-3 | 2,0 × 10-3 | 5,0 × 10-5 |
| 3 | 10,0 × 10-3 | 4,0 × 10-3 | 10,0 × 10-5 |
- 1. 1.
- 2. 2.
- 3. 3.
- 4. 4.
Explicación:
Para determinar el orden global, primero debemos hallar los órdenes parciales respecto a cada reactivo usando el método de las velocidades iniciales. La ecuación de velocidad tiene la forma:
v = k [NO]x [H2]y
- 1. Orden respecto al NO (x):Comparamos los Experimentos 1 y 2, donde [H2] es constante (2,0 × 10-3 M):
- – [NO] pasa de 5,0 a 10,0 (se duplica, ×2).
- – La velocidad pasa de 1,3 a 5,0 (aproximadamente se cuadriplica, ×4).
- – Matemáticamente: (2)x = 4 ⇒ x = 2.
- La reacción es de segundo orden respecto al NO.
- 2. Orden respecto al H2 (y):Comparamos los Experimentos 2 y 3, donde [NO] es constante (10,0 × 10-3 M):
- – [H2] pasa de 2,0 a 4,0 (se duplica, ×2).
- – La velocidad pasa de 5,0 a 10,0 (se duplica, ×2).
- – Matemáticamente: (2)y = 2 ⇒ y = 1.
- La reacción es de primer orden respecto al H2.
- 3. Orden Global:El orden global es la suma de los órdenes parciales:Orden Total = x + y = 2 + 1 = 3.
Pregunta 145
El potencial químico, μi:
- 1. Se puede utilizar como un criterio de equilibrio.
- 2. Es función de la temperatura y presión.
- 3. Es función de la temperatura y composición.
- 4. Se puede considerar como una propiedad extensiva.
Análisis de la Anulación:
Esta pregunta fue impugnada debido a la ambigüedad y la existencia de múltiples respuestas correcta o parcialmente correctas, dependiendo del contexto (sustancia pura vs. mezcla).
- • Opción 1 (Correcta): El potencial químico es fundamental en termodinámica porque la condición de equilibrio material (fases o reacción química) se alcanza cuando los potenciales químicos de cada componente son iguales en todas las fases. Por tanto, es estrictamente un criterio de equilibrio.
- • Análisis de las Variables (Opciones 2 y 3):
- – El potencial químico (μi) se define como la energía libre de Gibbs molar parcial.
- – Funcionalmente, depende de la Temperatura (T), la Presión (P) y la Composición (xi).
- – Opción 2: Dice que es función de T y P. Esto es cierto (siempre depende de ellas), pero incompleto para mezclas. Para una sustancia pura, es totalmente cierto.
- – Opción 3: Dice que es función de T y composición. También es cierto, pero incompleto (falta la presión).
- • Opción 4 (Falsa): El potencial químico es una propiedad intensiva (energía por mol), no extensiva.
Pregunta 146
El punto de ebullición de una sustancia se define como:
- 1. La temperatura a la que la presión de vapor de la sustancia iguala a la presión externa.
- 2. La temperatura a la que la presión de vapor de la sustancia es 1 bar.
- 3. La temperatura a la que la presión de vapor de la sustancia es 1 atm.
- 4. La temperatura a la cual la presión de vapor de la sustancia se mantiene constante.
Explicación:
La ebullición es el paso tumultuoso de líquido a gas que ocurre en toda la masa del líquido, no solo en la superficie.
- • La Definición Física (Opción 1 – Correcta):
- – Para que se forme una burbuja de vapor dentro del líquido y esta no colapse, la presión dentro de la burbuja (presión de vapor a esa Tª) debe ser capaz de vencer a la presión que la aplasta desde fuera (presión externa o atmosférica).
- – Por tanto, el punto de ebullición varía con la altura. En la cima del Everest (menor presión externa), el agua hierve a unos 70 ºC porque su presión de vapor iguala a la externa antes.
- • Distinción de términos (Opciones 2 y 3):
- – Punto de Ebullición Normal: Es el caso específico cuando la presión externa es 1 atm (760 mmHg).
- – Punto de Ebullición Estándar: Es el caso específico cuando la presión externa es 1 bar.
Pregunta 147
Los tensoactivos o surfactantes son sustancias:
- 1. Que tienden a estar fuertemente solvatadas, teniendo fuertes interacciones soluto-disolvente.
- 2. Que hacen que la tensión superficial disminuya con la concentración, ya que el soluto tiende a acumularse en la superficie.
- 3. Que hacen que la tensión superficial aumente con respecto al disolvente puro, y tanto más cuanto mayor sea la concentración de soluto.
- 4. Como el cloruro sódico, que tendrán fuertes interacciones de las partículas de soluto entre sí y su situación energética será más estable en el seno de la disolución que en la superficie.
Explicación:
Los surfactantes (agentes de superficie activa) son moléculas anfipáticas: poseen una cabeza polar (hidrófila) y una cola apolar (hidrófoba).
- • Mecanismo de Acción (Opción 2 – Correcta):
- – La parte hidrófoba «huye» del agua y busca la interfase aire-agua.
- – Al acumularse en la superficie (adsorción positiva), las moléculas de surfactante se intercalan entre las moléculas de agua.
- – Esto rompe la red de enlaces de hidrógeno superficiales (fuerzas de cohesión) que crean la tensión superficial del agua pura, provocando su disminución drástica.
- • Contraste con electrolitos (Opción 4):
- – Sustancias como el NaCl (sales inorgánicas) se hidratan fuertemente en el seno de la disolución.
- – «Huyen» de la superficie hacia el interior (adsorción negativa), lo que provoca un ligero aumento de la tensión superficial, justo lo contrario a un surfactante.
Pregunta 148
¿Con cuál de estas disoluciones se puede calibrar un conductímetro?:
- 1. Tampón o buffer.
- 2. Cloruro potásico.
- 3. Hidrogenoftalato de potasio.
- 4. Ácido benzoico.
Explicación:
La calibración de un conductímetro consiste en determinar la constante de celda (K), ya que la geometría exacta de los electrodos puede variar con el uso.
- • El Estándar de Referencia (Opción 2 – Correcta):
- – Las disoluciones de Cloruro de Potasio (KCl) son el estándar internacional aceptado para la conductividad.
- – Existen tablas precisas que relacionan la concentración de KCl (ej. 0.01 M, 0.1 M) con su conductividad específica a diferentes temperaturas (ej. 1413 µS/cm a 25 °C).
- – Al medir una solución de valor conocido, el equipo ajusta el factor de celda para que la lectura coincida con el valor teórico.
- • Uso de las otras sustancias:
- – Opciones 1 y 3: Los tampones y el hidrogenoftalato de potasio se usan para calibrar pH-metros, no conductímetros. Su conductividad no es el parámetro certificado.
- – Opción 4: El ácido benzoico es un patrón primario común en calorimetría (para calibrar bombas calorimétricas) o en valoraciones ácido-base, pero no en conductimetría.
Pregunta 149
En espectrofotometría de Ultravioleta (UV)-Visible (Vis):
- 1. Las cubetas de cuarzo no transmiten la luz visible, por lo que solo resultan útiles para medidas en la región de la longitud de onda UV.
- 2. Las cubetas de cuarzo y vidrio se limpian con una disolución de ácido fluorhídrico al 1 %.
- 3. Las cubetas de plástico en general no transmiten la luz UV, por lo que solo resultan útiles para medidas en la región de la longitud de onda visible.
- 4. La longitud de onda se expresa en nm-1 (nm = nanómetros).
Explicación:
La selección del material de la cubeta es crítica y depende del rango espectral en el que se va a trabajar.
- • Transparencia de Materiales (Opción 3 – Correcta):
- – Vidrio y Plástico estándar: Son transparentes en el Visible (380-780 nm) pero absorben fuertemente la radiación UV (por debajo de 350 nm). Por eso no sirven para medir ácidos nucleicos o proteínas en el UV.
- – Cuarzo (Sílice fundida): Es transparente tanto en el UV como en el Visible. (Contradice la Opción 1). Se puede usar para todo el rango, aunque es más caro.
- • Errores en las otras opciones:
- – Opción 2: ¡Peligro! El ácido fluorhídrico (HF) ataca y disuelve el vidrio y el cuarzo (SiO2). Usarlo destruiría las cubetas irremediablemente.
- – Opción 4: La longitud de onda (λ) es una distancia, se mide en nm. La unidad nm-1 (o cm-1) corresponde al número de onda (ν), que es el inverso de la longitud de onda.
Pregunta 150
¿Cuál es la configuración electrónica del Magnesio?:
- 1. 1s2 2s2 2p6 3s2.
- 2. [Ar] 4s2.
- 3. 1s2 2s2 2p6 3s2 3p2.
- 4. [Ar] 4s2 3d10 4p2.
Explicación:
Para determinar la configuración electrónica, necesitamos conocer el número atómico (Z) del elemento, que indica el número de protones y, en un átomo neutro, el número de electrones.
- • Análisis del Magnesio (Mg):
- – El Magnesio es un metal alcalinotérreo del Grupo 2, Periodo 3.
- – Su número atómico es Z = 12.
- – Llenado de orbitales (Principio de Aufbau): 1s (2 e–) → 2s (2 e–) → 2p (6 e–) → 3s (2 e–).
- – Suma total: 2 + 2 + 6 + 2 = 12 electrones. Esto corresponde exactamente a la Opción 1.
- • Identificación de las otras opciones:
- – Opción 2 ([Ar] 4s2): Corresponde al Calcio (Ca, Z=20).
- – Opción 3 (…3s2 3p2): Corresponde al Silicio (Si, Z=14).
- – Opción 4 ([Ar] … 4p2): Corresponde al Germanio (Ge, Z=32).
Pregunta 151
La presión osmótica se caracteriza por:
- 1. No depender del número y sí del tipo de partículas de soluto y por tanto es una propiedad coligativa.
- 2. Depender del número y no del tipo de partículas de soluto y por tanto es una propiedad no coligativa.
- 3. Depender del número y no del tipo de partículas de soluto y por tanto es una propiedad coligativa.
- 4. Depender tanto del número y del tipo de partículas de soluto y por tanto es una propiedad no coligativa.
Explicación:
Las propiedades de las disoluciones se clasifican en constitutivas (dependen de la naturaleza química) y coligativas.
- • Definición de Propiedad Coligativa (Opción 3 – Correcta):
- – El término proviene del latín colligare (reunir).
- – Estas propiedades (descenso de la presión de vapor, aumento ebulloscópico, descenso crioscópico y presión osmótica) dependen exclusivamente del número de partículas de soluto disueltas en una cantidad dada de disolvente.
- – La naturaleza química (tipo) de la partícula (si es urea, glucosa o un ión sodio) es irrelevante; solo importa «cuántas» hay.
- • Análisis de las opciones falsas:
- – Opción 1: Contradice la definición (dice que depende del tipo).
- – Opción 2: Describe bien la dependencia (solo número) pero concluye erróneamente que es «no coligativa».
- – Opción 4: Si dependiera del tipo, sería una propiedad constitutiva, no coligativa.
Pregunta 152
El número de orbitales moleculares formados:
- 1. Es el doble al número de orbitales atómicos que se combinan.
- 2. Es la mitad al número de orbitales atómicos que se combinan.
- 3. Es diferente del número de orbitales atómicos que se combinan.
- 4. Es igual al número de orbitales atómicos que se combinan.
Explicación:
Una de las reglas fundamentales de la Teoría de Orbitales Moleculares (TOM), basada en el método CLOA (Combinación Lineal de Orbitales Atómicos), es la conservación del número de orbitales.
- • Principio de Conservación (Opción 4 – Correcta):
- – Los orbitales no se crean ni se destruyen, solo se transforman.
- – Si combinamos N orbitales atómicos, obtendremos obligatoriamente N orbitales moleculares.
- – Generalmente, la mitad serán de menor energía (enlazantes) y la otra mitad de mayor energía (antienlazantes), pero la suma total siempre coincide con los orbitales de partida.
- • Ejemplo sencillo (H2):
- – Combinamos 1 orbital atómico (1s) del átomo A con 1 orbital atómico (1s) del átomo B.
- – Total orbitales atómicos = 2.
- – Resultado: 2 orbitales moleculares (σ1s y σ*1s).
Pregunta 153
¿Qué afirmación es VERDADERA de las fuerzas de London?:
- 1. Son de las fuerzas de atracción más fuertes descritas.
- 2. Únicamente están presentes en moléculas polares.
- 3. Se forman por las fluctuaciones en la distribución de electrones.
- 4. Son independientes del número de electrones de la molécula.
Explicación:
Las fuerzas de London (o de dispersión) son interacciones intermoleculares universales, presentes en todos los átomos y moléculas.
- • Mecanismo (Opción 3 – Correcta):
- – Aunque una molécula sea apolar en promedio, los electrones están en constante movimiento.
- – En un instante dado, la nube electrónica puede fluctuar y concentrarse más en un lado, creando un dipolo instantáneo.
- – Este dipolo induce otro dipolo en la molécula vecina (dipolo inducido), generando una atracción débil y efímera.
- • Errores en las otras opciones:
- – Opción 1: Son las fuerzas más débiles (comparadas con iónicas, covalentes o puente de hidrógeno).
- – Opción 2: Están presentes en todas las moléculas (polares y no polares). En las apolares son la única fuerza existente.
- – Opción 4: Dependen directamente de la polarizabilidad, la cual aumenta con el tamaño y el número de electrones. (Por eso el I2 es sólido y el F2 es gas).
Pregunta 154
La energía libre de Gibbs se define como una función de estado y sirve para determinar la espontaneidad de un proceso o reacción química. Según su definición, depende de tres variables que son:
- 1. La entalpia, la temperatura y la presión.
- 2. La entalpia, la presión y el volumen.
- 3. La temperatura, la presión y la entropía.
- 4. La entalpia, la temperatura y la entropía.
Explicación:
Para responder correctamente, debemos acudir a la ecuación matemática que define esta función termodinámica.
- • La Ecuación de Definición (Opción 4 – Correcta):
- – La Energía Libre de Gibbs (G) se define como:
- G = H – T·S
- – Donde los términos son:
- H = Entalpía. T = Temperatura absoluta. S = Entropía.
- • Aclaración conceptual:
- – Aunque a menudo decimos que G es función de la Presión y la Temperatura (sus «variables naturales» en la ecuación diferencial dG = VdP – SdT), la pregunta especifica explícitamente «según su definición«.
- – La definición constructiva combina el término energético (Entalpía) con el término desordenante (Entropía) modulado por la Temperatura.
Pregunta 155
El principio de incertidumbre de Heisenberg se basa en la descripción del momentum y la posición de una determinada masa “m” en el espacio. Según este principio cual es la afirmación VERDADERA:
- 1. El momentum y la posición de una determinada partícula “m” puede ser conocido junto a la onda asociada.
- 2. Es posible conocer el momentum y la posición de una determinada partícula “m” siempre y cuando se defina la onda asociada.
- 3. Es imposible especificar simultáneamente, con precisión, ambos, el momentum y la posición de una partícula “m”.
- 4. Es posible especificar el momentum y la posición de una partícula “m” mediante el uso de la ecuación de Schrödinger.
Explicación:
El Principio de Incertidumbre de Heisenberg (1927) es una consecuencia fundamental de la dualidad onda-partícula y establece un límite intrínseco a la precisión de las medidas en el mundo cuántico.
- • La Relación Matemática (Opción 3 – Correcta):
- – La expresión es: Δx · Δp ≥ h / 4π.
- – Donde Δx es la incertidumbre en la posición y Δp es la incertidumbre en el momento lineal (cantidad de movimiento).
- – Esto significa que cuanto más precisamente conozcamos la posición (Δx pequeño), mayor será obligatoriamente la incertidumbre sobre su velocidad/momento (Δp grande), y viceversa. Es imposible conocer ambos valores exactos al mismo tiempo.
- • Descarte de otras opciones:
- – Opciones 1 y 2: Sugieren que sí es posible conocer ambos, lo cual contradice directamente el principio. Definir la onda (función de onda) nos da probabilidades, no certezas simultáneas de variables conjugadas.
- – Opción 4: La ecuación de Schrödinger describe la evolución temporal de la función de onda, pero no elimina la incertidumbre inherente al intentar medir las observables posición y momento simultáneamente.
Pregunta 156
La ecuación que define el fenómeno fotofísico de la fluorescencia es: S* → S + hν. De igual forma, la ecuación que define el fenómeno fotofísico de la fosforescencia es: T* → S + hν. Teniendo en cuenta ambas definiciones, cuál de las siguientes afirmaciones es la VERDADERA:
- 1. La fluorescencia es un proceso más rápido que la fosforescencia.
- 2. La fosforescencia es un proceso más rápido que la fluorescencia.
- 3. Tanto la fluorescencia como la fosforescencia se producen en rangos de tiempo iguales.
- 4. La fluorescencia y la fosforescencia se producen de forma instantánea.
Explicación:
La diferencia cinética entre ambos fenómenos radica en la «probabilidad» de la transición electrónica según las reglas de selección de la mecánica cuántica.
- • Fluorescencia (S* → S):
- – Ocurre entre estados de la misma multiplicidad de espín (Singlete excitado a Singlete fundamental).
- – Es una transición «permitida» cuánticamente.
- – Por tanto, ocurre muy rápido. La vida media es típica del orden de 10-9 a 10-7 segundos (nanosegundos). Desaparece casi instantáneamente al apagar la fuente de excitación.
- • Fosforescencia (T* → S):
- – Ocurre entre estados de diferente multiplicidad (Triplete a Singlete). Implica un cambio de espín del electrón.
- – Es una transición «prohibida» por las reglas de selección. Solo ocurre gracias al acoplamiento espín-órbita.
- – Al ser poco probable, es un proceso lento. La vida media varía desde 10-4 segundos hasta varios segundos o incluso horas. Esta emisión retardada es lo que hace que brille en la oscuridad.
Pregunta 157
La constante de velocidad de primer orden de una reacción posee unidades de:
- 1. mol·dm-3·s-1.
- 2. mol-1·s-1.
- 3. dm3·mol-1·s-1.
- 4. s-1.
Explicación:
Las unidades de la constante de velocidad (k) dependen del orden global de la reacción, ya que deben asegurar que la velocidad resultante tenga siempre unidades de concentración/tiempo.
- • Deducción para Primer Orden (Opción 4):
- – La ecuación de velocidad es: v = k · [A]1.
- – Despejamos k: k = v / [A].
- – Sustituimos las unidades típicas:
- Unidades de v = mol·dm-3·s-1 (Molaridad/segundo)
- Unidades de [A] = mol·dm-3 (Molaridad)
- k = (mol·dm-3·s-1) / (mol·dm-3) = s-1.
- – Al ser de primer orden, la concentración se cancela y la constante tiene unidades de inversa de tiempo (tiempo-1).
- • Otras opciones:
- – Opción 1: Unidades de velocidad de reacción (orden cero).
- – Opción 3: Unidades de constante de segundo orden (M-1·s-1).
Pregunta 158
¿Con qué está relacionado el factor de probabilidad (P) en la teoría de colisiones?:
- 1. Con la entalpía de formación del complejo activado y la energía de activación.
- 2. Con la entropía de formación del complejo activado y la energía de activación.
- 3. Con la entalpía de formación del complejo activado.
- 4. Con la entropía de formación del complejo activado.
Explicación:
En la Teoría de Colisiones, la constante de velocidad se expresa como k = P · Z · exp(-Ea/RT), donde Z es la frecuencia de colisiones y P es el factor de probabilidad o estérico.
- • Significado físico de P (Factor Estérico):
- – P corrige el hecho de que no todas las colisiones con suficiente energía producen reacción; las moléculas deben chocar con la orientación adecuada.
- – Una orientación específica implica un alto grado de orden en el momento del choque para formar el complejo activado.
- • Conexión con la Termodinámica (Teoría del Estado de Transición):
- – Al comparar la ecuación de Arrhenius/Colisiones con la ecuación de Eyring (Termodinámica Estadística), el término pre-exponencial (donde está P) se corresponde con el término de Entropía de Activación (ΔS‡).
- – P ∝ exp(ΔS‡/R).
- – Si la reacción requiere una orientación muy precisa (P muy bajo), significa que el complejo activado es muy ordenado respecto a los reactivos, lo que implica una disminución de entropía (ΔS‡ negativa).
Pregunta 159
En el punto crítico, la isoterma en el diagrama P–V:
- 1. Tiene una pendiente constante.
- 2. Presenta una inflexión.
- 3. Corta al eje de presión.
- 4. Pasa por el origen.
Explicación:
El comportamiento de los gases reales se describe mediante las isotermas de Andrews en un diagrama Presión-Volumen (P-V).
- • Análisis Geométrico y Matemático (Opción 2 – Correcta):
- – Por debajo de la temperatura crítica (T < Tc), las isotermas presentan un tramo horizontal que representa la coexistencia de dos fases (líquido y vapor).
- – A medida que aumentamos la temperatura, este tramo horizontal se acorta hasta reducirse a un solo punto cuando T = Tc. Este es el Punto Crítico.
- – Matemáticamente, en este punto la isoterma se vuelve horizontal momentáneamente (pendiente nula) y cambia de curvatura (cóncava a convexa). Esto define un punto de inflexión horizontal.
- – Las condiciones son:1ª Derivada: (∂P / ∂V)T = 02ª Derivada: (∂2P / ∂V2)T = 0
- • Descarte de otras opciones:
- – Opción 1: La pendiente no es constante; varía a lo largo de toda la curva, siendo cero solo en el punto crítico.
- – Opciones 3 y 4: Son irrelevantes para la definición termodinámica del punto crítico.
Pregunta 160
¿Qué obtenemos si vaporizamos un líquido de composición azeotrópica?:
- 1. Un vapor más rico en el componente más volátil.
- 2. Un vapor más rico en el componente menos volátil.
- 3. Un vapor más rico en ambos componentes.
- 4. Un vapor de la misma composición que el líquido.
Explicación:
Un azeótropo (del griego «no cambia al hervir») es una mezcla líquida que se comporta como si fuera una sustancia pura en su punto de ebullición.
- • Comportamiento de Fase (Opción 4 – Correcta):
- – En una mezcla ideal (destilación simple), el vapor es siempre más rico en el componente más volátil (Opción 1).
- – Sin embargo, en el punto azeotrópico, las fuerzas intermoleculares causan una desviación tal que la curva del líquido y la del vapor se tocan.
- – Matemáticamente: xi (líquido) = yi (vapor). Al hervir, la composición no cambia, lo que impide la separación de los componentes mediante destilación simple.
- • Ejemplo Clásico:
- – El etanol al 96% en agua forma un azeótropo. Al hervirlo, el vapor resultante sigue siendo 96% etanol, por lo que no se puede obtener etanol puro (100%) sin técnicas especiales (como añadir benceno o cambiar la presión).
Pregunta 161
Si un líquido en contacto con un sólido forma una superficie cóncava, ¿cuál será el ángulo de contacto formado entre la superficie del sólido y la tangente a la superficie del líquido en el punto de contacto con el sólido?:
- 1. Inferior a 90º.
- 2. Superior a 90º.
- 3. Inferior a 180º.
- 4. Superior a 180º.
Explicación:
La forma del menisco (la superficie curva del líquido) depende del balance entre las fuerzas de cohesión (líquido-líquido) y las fuerzas de adhesión (líquido-sólido).
- • Menisco Cóncavo (Líquido que moja):
- – Ocurre cuando las fuerzas de adhesión > cohesión (ej. agua en vidrio). El líquido «trepa» por las paredes del recipiente.
- – El ángulo de contacto (θ) se mide desde la pared sólida hacia el interior del líquido.
- – Geométricamente, para que la curva suba por la pared (cóncava), la tangente debe formar un ángulo agudo, es decir, θ < 90º.
- • Menisco Convexo (Líquido que no moja):
- – Ocurre cuando cohesión > adhesión (ej. mercurio en vidrio). El líquido se retrae de las paredes.
- – En este caso, el ángulo es obtuso (θ > 90º).
Pregunta 162
¿Qué modelo de isoterma de adsorción predice saturación de todos los sitios activos?:
- 1. Langmuir.
- 2. Freundlich.
- 3. BET.
- 4. Langmuir y BET.
Explicación:
Las isotermas describen cómo interactúa un adsorbato (gas/líquido) con una superficie sólida a temperatura constante.
- • Modelo de Langmuir (Opción 1 – Correcta):
- – Se basa en la suposición de que la adsorción ocurre en una única capa (monocapa).
- – Asume que existe un número finito de sitios activos idénticos y que, una vez ocupados, no cabe más adsorbato.
- – Matemáticamente, la curva alcanza una asíntota horizontal ($q_{max}$), que corresponde a la saturación total de la superficie.
- • Diferencia con otros modelos:
- – BET (Brunauer–Emmett–Teller): Es una extensión de Langmuir que permite la formación de multicapas. Aunque la primera capa se satura, las siguientes continúan adsorbiendo indefinidamente al aumentar la presión (hasta la condensación), por lo que la curva no se aplana, sino que sube.
- – Freundlich: Es un modelo empírico para superficies heterogéneas que no asume un límite de saturación; la adsorción aumenta indefinidamente con la concentración.
Pregunta 163
La existencia de un gradiente de velocidad en un fluido origina:
- 1. Un flujo de electrones.
- 2. Un flujo de cantidad de movimiento.
- 3. Un flujo de materia.
- 4. Un flujo de energía.
Explicación:
En fisicoquímica, los fenómenos de transporte se rigen por leyes análogas donde una «fuerza impulsora» (gradiente) provoca un flujo.
- • Ley de Newton de la Viscosidad (Opción 2 – Correcta):
- – Si un fluido se mueve por capas a diferentes velocidades (existe un gradiente de velocidad dv/dy), las capas rápidas arrastran a las lentas y las lentas frenan a las rápidas.
- – Esta fricción interna implica una transferencia de cantidad de movimiento (momento lineal) perpendicular a la dirección del flujo.
- – La viscosidad es, de hecho, el coeficiente de difusión de cantidad de movimiento.
- • Comparación con otros transportes:
- – Flujo de Materia (Difusión): Originado por un gradiente de concentración (Ley de Fick).
- – Flujo de Energía (Calor): Originado por un gradiente de temperatura (Ley de Fourier).
- – Flujo de Electrones (Corriente): Originado por un gradiente de potencial eléctrico (Ley de Ohm).
Pregunta 164
En la Ley de Fick, entendida como la ecuación de la difusión como fenómeno de transporte, se relaciona:
- 1. El flujo de concentración con el gradiente de potencial químico.
- 2. El flujo de materia con el gradiente de potencial químico.
- 3. El flujo de materia con el gradiente temporal del número de moles de soluto.
- 4. El flujo de potencial químico con el gradiente de concentración.
Explicación:
Para entender la difusión a un nivel fundamental, debemos ir más allá de la simplificación habitual y acudir a la termodinámica de procesos irreversibles.
- • La Ley Fenomenológica (Lo que solemos ver):
- – Habitualmente escribimos la 1ª Ley de Fick como: J = -D · (dc / dx).
- – Esto relaciona el flujo de materia (J) con el gradiente de concentración. Sin embargo, esto solo es estrictamente cierto en disoluciones ideales.
- • La Realidad Termodinámica (Opción 2 – Correcta):
- – La materia no se mueve simplemente porque haya «mucha cantidad» en un sitio, sino porque busca reducir su energía libre.
- – La verdadera fuerza impulsora es el gradiente de potencial químico (μ).
- – La ecuación generalizada es: J = – L · (dμ / dx).
- – Por tanto, la difusión relaciona el flujo de materia (moles moviéndose) con el gradiente de potencial químico (la diferencia de energía química que los empuja).
Pregunta 165
La viscosidad de un fluido newtoniano en movimiento es de 1 mPa·s. ¿Cuál será su viscosidad cuando el fluido esté en reposo?:
- 1. 0 mPa·s.
- 2. 0,5 mPa·s.
- 3. 1 mPa·s.
- 4. 2 mPa·s.
Explicación:
Esta pregunta evalúa el conocimiento sobre la definición reológica de los fluidos.
- • ¿Qué es un fluido Newtoniano? (Opción 3 – Correcta):
- – Es aquel que cumple la Ley de Newton de la viscosidad: τ = η · (dv/dy).
- – La característica clave es que su viscosidad (η) es una constante intrínseca del material a una temperatura y presión dadas.
- – No depende de la velocidad: La viscosidad no cambia si el fluido va rápido, lento o está quieto. Es una propiedad física como la densidad. Si es 1 mPa·s en movimiento, sigue siendo 1 mPa·s en reposo.
- • Comparación con fluidos No Newtonianos:
- – Pseudoplásticos: La viscosidad baja al agitarlo (ej. pintura, sangre).
- – Dilatantes: La viscosidad sube al agitarlo (ej. maicena).
- – En estos casos la viscosidad sí cambiaría al pasar del movimiento al reposo, pero el enunciado especifica «Newtoniano».
Pregunta 166
En relación con los ácidos grasos, señale la afirmación VERDADERA:
- 1. Los ácidos grasos saturados contienen uno o más dobles enlaces.
- 2. La insaturación provoca un aumento del punto de fusión.
- 3. Los ácidos grasos insaturados naturales suelen tener dobles enlaces en configuración cis.
- 4. Los dobles enlaces trans son los más comunes en los lípidos biológicos naturales.
Explicación:
La estructura química de los ácidos grasos determina sus propiedades físicas y su función en las membranas biológicas.
- • Configuración Natural (Opción 3 – Correcta):
- – En la naturaleza, casi todos los ácidos grasos insaturados presentan sus dobles enlaces en configuración cis.
- – Esta configuración introduce un «codo» o curvatura rígida en la cadena hidrocarbonada, lo que impide que las moléculas se empaqueten estrechamente.
- – Esta falta de empaquetamiento aumenta la fluidez de la membrana, una característica vital para las células.
- • Errores en las otras opciones:
- – Opción 1: Los saturados tienen enlaces simples (están «saturados» de hidrógeno). Los insaturados tienen dobles enlaces.
- – Opción 2: La insaturación (especialmente cis) disminuye el punto de fusión. Por eso el aceite de oliva (insaturado) es líquido y la mantequilla (saturada) es sólida.
- – Opción 4: Los enlaces trans son raros en la naturaleza (producidos principalmente por hidrogenación industrial o bacterias ruminales) y se comportan más como grasas saturadas.
Pregunta 167
¿Cuál de las siguientes afirmaciones es VERDADERA respecto al ciclo de Krebs?:
- 1. Se produce principalmente en el retículo endoplasmático.
- 2. Su función es la producción de energía en forma de ATP.
- 3. Utiliza NADH como sustrato.
- 4. Durante el proceso no se sintetiza citrato.
Explicación:
El Ciclo de Krebs (o del Ácido Cítrico) es la ruta central del metabolismo aerobio, donde convergen las vías de degradación de carbohidratos, grasas y proteínas.
[Image of ciclo de krebs mitocondria]- • Función Energética (Opción 2 – Correcta):
- – El objetivo principal del ciclo es oxidar el Acetil-CoA para liberar energía.
- – Produce energía directamente en forma de GTP (que se convierte fácilmente en ATP).
- – Sobre todo, genera poder reductor (NADH y FADH2) que alimentará la cadena de transporte electrónico para producir grandes cantidades de ATP mediante fosforilación oxidativa.
- • Corrección de las otras opciones:
- – Opción 1: Ocurre en la matriz mitocondrial (en eucariotas), no en el retículo.
- – Opción 3: El NADH es un producto del ciclo, no un sustrato. El sustrato oxidado es el NAD+.
- – Opción 4: La primera reacción del ciclo, catalizada por la citrato sintasa, es precisamente la síntesis de citrato a partir de oxalacetato y Acetil-CoA.
Pregunta 168
¿En qué proceso metabólico son esenciales las reacciones de transaminación?:
- 1. Degradación de aminoácidos.
- 2. Metabolismo de ácidos grasos.
- 3. Vía de las pentosas fosfato.
- 4. Glucolisis.
Explicación:
El catabolismo de los aminoácidos requiere un paso previo fundamental antes de que su esqueleto de carbono pueda ser oxidado para obtener energía.
- • El Mecanismo de Transaminación (Opción 1 – Correcta):
- – Consiste en la transferencia del grupo α-amino de un aminoácido a un α-cetoácido (generalmente α-cetoglutarato).
- – Esta reacción es catalizada por las transaminasas (o aminotransferasas) y utiliza piridoxal fosfato (vitamina B6) como cofactor.
- – Objetivo: Separar el nitrógeno (que irá al ciclo de la urea como glutamato/amonio) del esqueleto carbonado (α-cetoácido), el cual ingresará al ciclo de Krebs o a la gluconeogénesis. Sin este paso, el aminoácido no puede degradarse.
- • Descarte de otras vías:
- – Ácidos grasos (β-oxidación): Se degradan cortando unidades de dos carbonos (Acetil-CoA), no implican manejo de nitrógeno.
- – Glucolisis y Pentosas Fosfato: Son rutas del metabolismo de carbohidratos (C, H, O), donde no intervienen grupos amino.
Pregunta 169
¿Qué son los aptámeros?:
- 1. Son oligómeros de proteínas que se unen con elevada especificidad a la diana molecular.
- 2. Son oligómeros de ácidos nucleicos que se unen con elevada afinidad a su diana molecular.
- 3. Son anticuerpos de pequeño tamaño con baja afinidad por la diana molecular.
- 4. Son oligosacáridos sintéticos con propiedades inmunogénicas.
Explicación:
El término «aptámero» deriva del latín aptus (encajar) y describe una clase de moléculas capaces de reconocer dianas con altísima precisión.
- • Definición Química y Funcional (Opción 2 – Correcta):
- – Son cadenas cortas de ácidos nucleicos (ADN o ARN de cadena sencilla), típicamente de 20 a 60 nucleótidos.
- – Tienen la capacidad de plegarse en estructuras tridimensionales complejas (horquillas, bucles, G-cuádruplex).
- – Esta forma 3D les permite unirse a su diana (proteínas, fármacos, células) con una afinidad y especificidad comparable o superior a la de los anticuerpos monoclonales.
- • Diferencias clave con los distractores:
- – No son proteínas (Opción 1 y 3): A diferencia de los anticuerpos o péptidos, los aptámeros se sintetizan químicamente (método SELEX), no biológicamente, lo que reduce la variabilidad entre lotes.
- – No son azúcares (Opción 4): Su esqueleto es fosfato-azúcar-base nitrogenada.
Pregunta 170
¿Cuál de los siguientes complejos moleculares se encarga de la replicación del ADN?:
- 1. Replicón.
- 2. Espliceosoma.
- 3. Replisoma.
- 4. Ribosoma.
Explicación:
La replicación del ADN no es tarea de una sola enzima, sino de una enorme «máquina» multiproteica que coordina varias funciones simultáneas (desenrollar, mantener hebras separadas, sintetizar, corregir).
- • El Replisoma (Opción 3 – Correcta):
- – Es el complejo supramolecular situado en la horquilla de replicación.
- – Integra a la Helicasa (abre la hélice), la Primasa (sintetiza cebadores), las ADN Polimerasas (sintetizan la nueva hebra), las proteínas de unión a cadena sencilla (SSB) y la abrazadera deslizante (clamp).
- – Funciona como una unidad coordinada para duplicar el genoma con alta fidelidad.
- • Diferenciación de términos:
- – Replicón (Opción 1): Es la unidad de ADN que se replica a partir de un único origen. En bacterias hay un solo replicón; en eucariotas, miles. (Es el «objeto», no el «sujeto»).
- – Espliceosoma (Opción 2): Complejo ribonucleoproteico encargado del corte y empalme (splicing) del ARN mensajero, eliminando intrones.
- – Ribosoma (Opción 4): Complejo encargado de la traducción (síntesis de proteínas), no de la replicación.
Pregunta 171
¿Cuál de las siguientes alteraciones estructurales cromosómicas corresponde al intercambio de segmentos entre dos cromosomas no homólogos?:
- 1. Translocaciones.
- 2. Inversiones.
- 3. Isocromosomas.
- 4. Deleciones.
Explicación:
Las anomalías cromosómicas estructurales implican roturas y reordenamientos. La clave para identificarlas es ver «quién» intercambia material con «quién».
- • Translocación (Opción 1 – Correcta):
- – Se define como la transferencia de un segmento de un cromosoma a otro cromosoma no homólogo (ej. del cromosoma 9 al 22, causando la leucemia mieloide crónica).
- – Puede ser recíproca (intercambio mutuo) o no recíproca.
- – Nota: Si el intercambio fuera entre homólogos, sería recombinación normal (crossing-over).
- • Otras alteraciones:
- – Inversiones (Opción 2): Ocurren dentro del mismo cromosoma. Un segmento se rompe, gira 180º y se vuelve a unir (ABCD → ACBD).
- – Isocromosomas (Opción 3): Error en la división del centrómero (transversal en vez de longitudinal), resultando en un cromosoma con dos brazos idénticos (ej. dos brazos largos y ningún corto).
- – Deleciones (Opción 4): Pérdida neta de un fragmento de ADN.
Pregunta 172
¿Qué método se utiliza para detectar ARNm de forma cuantitativa?:
- 1. Electroforesis en gel de agarosa.
- 2. Southern blot.
- 3. PCR con enzimas de restricción.
- 4. PCR en tiempo real.
Explicación:
Para cuantificar la expresión génica (niveles de ARNm), necesitamos una técnica que mida la cantidad de molde inicial con precisión.
- • RT-qPCR (PCR Cuantitativa en Tiempo Real) (Opción 4 – Correcta):
- – Primero, el ARNm se retrotranscribe a ADNc (RT).
- – Luego, durante la amplificación por PCR, se utilizan sondas fluorescentes (como SYBR Green o TaqMan).
- – El termociclador mide la fluorescencia en cada ciclo. El ciclo en el que la fluorescencia supera el umbral (Ct) es inversamente proporcional a la cantidad inicial de ARNm. Esto permite una cuantificación absoluta o relativa muy precisa.
- • Por qué no las otras:
- – Electroforesis (Opción 1): Es cualitativa o semicuantitativa (ver una banda más gorda que otra), pero tiene poca resolución y rango dinámico.
- – Southern blot (Opción 2): Detecta secuencias de ADN, no de ARN (para ARN sería Northern blot).
- – PCR con restricción (Opción 3): Se usa para genotipado (RFLP) o clonación, no para cuantificar expresión.
Pregunta 173
¿Cuál de las siguientes técnicas de edición genética permite la inserción controlada de un gen de interés, en una ubicación específica del genoma (knock-in)?:
- 1. CRISPR (repeticiones palindrómicas cortas agrupadas y regularmente interespaciadas).
- 2. Enzimas de restricción.
- 3. Mutagénesis de sitio dirigido.
- 4. ARN pequeño de interferencia (siRNA).
Explicación:
La tecnología CRISPR/Cas9 ha revolucionado la ingeniería genética por su capacidad de programar cortes precisos en el genoma de células vivas.
- • Mecanismo de Knock-in (Opción 1 – Correcta):
- – El sistema utiliza un ARN guía (sgRNA) para dirigir la nucleasa Cas9 al sitio exacto del genoma donde queremos editar.
- – La Cas9 corta el ADN (rotura de doble cadena).
- – Si suministramos un fragmento de ADN molde externo (plantilla) que contenga el gen de interés flanqueado por secuencias homólogas, la célula reparará el corte copiando e insertando este nuevo gen mediante Recombinación Homóloga (HDR).
- – Esto crea un «Knock-in» (inserción dirigida).
- • Descarte de otras opciones:
- – siRNA (Opción 4): Provoca el silenciamiento transitorio («Knock-down») degradando el ARNm, pero no altera la secuencia del ADN genómico.
- – Mutagénesis dirigida (Opción 3): Se usa in vitro sobre plásmidos (vectores), no directamente para inserciones genómicas complejas in vivo.
Pregunta 174
La fosforilación de la glucosa a glucosa-6-fosfato que tiene lugar en la glucólisis está catalizada por:
- 1. Glucosa-6-fosfatasa.
- 2. Fructoquinasa.
- 3. Hexoquinasa.
- 4. Fosforilasa quinasa.
Explicación:
El primer paso de la glucólisis es una reacción de preparación fundamental para «atrapar» la glucosa dentro de la célula y activarla para su posterior rotura.
- • La Reacción (Opción 3 – Correcta):
- – Glucosa + ATP → Glucosa-6-P + ADP.
- – Esta transferencia de un grupo fosfato es catalizada por la Hexoquinasa (o la Glucoquinasa en el hígado). Es una reacción irreversible que consume energía.
- – Al tener carga negativa, la G6P ya no puede atravesar la membrana y salir de la célula.
- • Análisis de las otras enzimas:
- – Glucosa-6-fosfatasa (Opción 1): Cataliza justo la reacción inversa (quita el fosfato) durante la gluconeogénesis. Solo está presente en hígado y riñón para liberar glucosa a la sangre.
- – Fructoquinasa (Opción 2): Fosforila fructosa, no glucosa.
- – Fosforilasa quinasa (Opción 4): Regula la degradación del glucógeno activando a la glucógeno fosforilasa.
Pregunta 175
¿Cuál es la función principal de la vía de la pentosa fosfato?:
- 1. Síntesis de Ribosa y fuente de NADPH.
- 2. Produce glucosa y elimina lactato y glicerol.
- 3. Descompone glucosa.
- 4. Descompone ácidos grasos y produce ATP.
Explicación:
La vía de las pentosas fosfato es una ruta alternativa a la glucólisis que no busca obtener ATP, sino satisfacer necesidades biosintéticas.
- • Productos Principales (Opción 1 – Correcta):
- – NADPH: Poder reductor esencial para la síntesis de ácidos grasos, colesterol y para combatir el estrés oxidativo (glutatión).
- – Ribosa-5-fosfato: Azúcar de 5 carbonos necesario para sintetizar nucleótidos (ADN, ARN) y coenzimas.
- • Diferenciación de otras rutas:
- – Opción 2: Describe la Gluconeogénesis (sintetizar glucosa nueva a partir de precursores no glucídicos).
- – Opción 3: Aunque oxida glucosa, su fin no es la descomposición total para energía (como el ciclo de Krebs), sino la interconversión de azúcares.
- – Opción 4: Describe la β-oxidación de los ácidos grasos.
Pregunta 176
¿Cuál de los siguientes aminoácidos se considera esencial para la dieta?:
- 1. Asparagina.
- 2. Valina.
- 3. Prolina.
- 4. Serina.
Explicación:
Los aminoácidos esenciales son aquellos que el organismo humano no puede sintetizar de novo y, por tanto, deben ser ingeridos obligatoriamente con la dieta.
- • La Valina (Opción 2 – Correcta):
- – Es un aminoácido de cadena ramificada (BCAA), junto con la Leucina y la Isoleucina.
- – Pertenece al grupo de los 9 esenciales: Histidina, Isoleucina, Leucina, Lisina, Metionina, Fenilalanina, Treonina, Triptófano y Valina.
- • Descarte de los no esenciales:
- – Asparagina, Prolina y Serina: El cuerpo puede sintetizarlos a partir de intermediarios metabólicos (como el oxalacetato o el 3-fosfoglicerato), por lo que no es vital consumirlos directamente.
Pregunta 177
Selecciona la respuesta VERDADERA respecto a la hemoglobina:
- 1. Es una lipoproteína.
- 2. Posee en su estructura un átomo de Aluminio.
- 3. La Hemoglobina A del adulto está formada por cuatro cadenas polipeptídicas: dos alfa y dos beta.
- 4. La Hemoglobina F está formada por cuatro cadenas polipeptídicas: dos alfa y dos delta.
Explicación:
La hemoglobina es una proteína globular con estructura cuaternaria (tetrámero) encargada del transporte de oxígeno.
- • Estructura de la HbA (Opción 3 – Correcta):
- – La Hemoglobina A (Adulto mayoritaria, >95%) es un heterotetrámero formado por dos cadenas de globina tipo α y dos cadenas de globina tipo β (α2β2).
- • Análisis de errores:
- – Opción 1: Es una hemoproteína (grupo prostético hemo), no una lipoproteína (no transporta lípidos).
- – Opción 2: El átomo central del grupo hemo es Hierro (Fe2+), no Aluminio.
- – Opción 4: La Hemoglobina F (Fetal) es α2γ2 (gamma). La combinación α2δ2 (delta) corresponde a la Hemoglobina A2 (minoritaria en adultos).
Pregunta 178
En el ciclo del ácido cítrico o ciclo de los ácidos tricarboxílicos, el producto resultante de la reacción entre acetil-CoA y Oxaloacetato es:
- 1. Citrato.
- 2. Isocitrato.
- 3. α-Cetoglutarato.
- 4. Fructosa-1-fosfato.
Explicación:
Esta es la reacción que «alimenta» el ciclo e inicia la oxidación de los carbonos provenientes de la glucólisis o beta-oxidación.
- • La Reacción de la Citrato Sintasa (Opción 1 – Correcta):
- – Es una condensación aldólica seguida de hidrólisis.
- – Reactivos: Acetil-CoA (2 carbonos) + Oxalacetato (4 carbonos).
- – Producto: Citrato (6 carbonos, ácido tricarboxílico) + Coenzima A libre.
- – Es una reacción irreversible que marca el «punto de no retorno» del ciclo.
- • Secuencia posterior:
- – El citrato luego se isomeriza a Isocitrato (Opción 2), el cual se oxida a α-Cetoglutarato (Opción 3). La Fructosa-1-P es de la vía de la fructosa, no de Krebs.
Pregunta 179
El ácido úrico es un producto de la degradación de:
- 1. Aminoácidos aromáticos.
- 2. Bases púricas.
- 3. Colesterol.
- 4. Glicolípidos.
Explicación:
El metabolismo de los ácidos nucleicos implica el reciclaje o la eliminación de sus bases nitrogenadas constituyentes.
- • Catabolismo de Purinas (Opción 2 – Correcta):
- – Las purinas principales (Adenina y Guanina) se degradan a través de intermediarios como la hipoxantina y la xantina.
- – La enzima Xantina Oxidasa cataliza el paso final oxidando la xantina a Ácido Úrico.
- – En humanos y primates, este es el producto final de excreción (somos ureotélicos para el nitrógeno proteico, pero uricotélicos para las purinas). Su acumulación excesiva provoca gota.
- • Comparación con otros productos:
- – Aminoácidos: Su nitrógeno se excreta como Urea (ciclo de la urea).
- – Colesterol: Se elimina como ácidos biliares.
- – Bases Pirimidínicas: Se degradan a compuestos solubles (beta-alanina, beta-aminoisobutirato, CO2 y NH3), no a ácido úrico.
Pregunta 180
¿Cómo se llama el mecanismo mediante el cual se sintetiza RNA a partir de DNA?:
- 1. Traducción.
- 2. Replicación.
- 3. Transcripción.
- 4. Duplicación replicacional.
Explicación:
Este proceso es el primer paso de la expresión génica, regido por el Dogma Central de la Biología Molecular.
- • Definición de Procesos (Opción 3 – Correcta):
- – Transcripción: Es la síntesis de una cadena de ARN (mensajero, ribosómico o de transferencia) usando una hebra de ADN como molde. La enzima clave es la ARN polimerasa. Se llama así porque «transcribimos» el mensaje del mismo idioma (ácidos nucleicos) a un dialecto ligeramente distinto (ADN a ARN).
- • Los otros pasos:
- – Replicación (Opción 2): Síntesis de ADN a partir de ADN (copia).
- – Traducción (Opción 1): Síntesis de Proteínas a partir de ARNm. Aquí se «traduce» el mensaje de un idioma de 4 letras (nucleótidos) a uno de 20 letras (aminoácidos).
Pregunta 181
¿Qué enzima se encarga de unir los fragmentos cortos de ADN producidos durante la replicación de la cadena retardada del ADN?:
- 1. Helicasa.
- 2. Primasa.
- 3. Ligasa.
- 4. Topoisomerasa.
Explicación:
En la hebra retardada (discontinua), la ADN polimerasa solo puede sintetizar en dirección 5’→3′, alejándose de la horquilla, lo que genera pequeños trozos llamados Fragmentos de Okazaki.
- • Acción de la ADN Ligasa (Opción 3 – Correcta):
- – Una vez que la ADN polimerasa I elimina los cebadores de ARN y rellena los huecos con ADN, queda una melladura («nick») en el esqueleto azúcar-fosfato entre los fragmentos adyacentes.
- – La Ligasa cataliza la formación de un enlace fosfodiéster covalente entre el extremo 3′-OH de un fragmento y el 5′-P del siguiente, consumiendo ATP (o NAD+ en bacterias).
- – Esto convierte los fragmentos sueltos en una cadena continua.
- • Funciones de las otras enzimas:
- – Helicasa (Opción 1): Rompe los puentes de hidrógeno para separar las dos hebras («abre la cremallera»).
- – Primasa (Opción 2): Sintetiza el cebador (primer) de ARN necesario para iniciar la síntesis.
- – Topoisomerasa (Opción 4): Relaja la tensión de torsión (superenrollamiento) por delante de la horquilla.
Pregunta 182
La estructura primaria de las proteínas:
- 1. Es única y característica de cada proteína y está determinada por los genes.
- 2. Es la secuencia de aminoácidos de una proteína, que se describe empezando por el extremo carboxilo.
- 3. Se refiere a patrones regulares de estructura que se repiten en las proteínas, como la hélice α y la conformación β.
- 4. La desnaturalización conlleva la pérdida de esta estructura.
Explicación:
La estructura de una proteína se organiza en niveles jerárquicos, siendo la primaria la base de todas las demás.
- • Definición (Opción 1 – Correcta):
- – La estructura primaria es la secuencia lineal exacta de aminoácidos unidos por enlaces peptídicos.
- – Esta secuencia viene dictada directamente por la secuencia de nucleótidos del gen correspondiente (Dogma Central).
- – Es única para cada proteína y contiene toda la información necesaria para que esta se pliegue en su forma tridimensional funcional.
- • Análisis de errores:
- – Opción 2: Por convención internacional, las secuencias se leen siempre desde el extremo Amino-terminal (N) hacia el Carboxilo-terminal (C), igual que la síntesis en el ribosoma.
- – Opción 3: Describe la estructura secundaria (plegamiento local).
- – Opción 4: La desnaturalización rompe los enlaces débiles (H, iónicos, hidrofóbicos), destruyendo las estructuras 2ª, 3ª y 4ª, pero mantiene intacta la estructura primaria (enlaces peptídicos covalentes).
Pregunta 183
¿De qué clase es la enzima hexoquinasa?:
- 1. Clase 1. Oxidorreductasa.
- 2. Clase 2. Transferasa.
- 3. Clase 3. Hidrolasa.
- 4. Clase 4. Liasa.
Explicación:
Las enzimas se clasifican en 6 grandes grupos según el tipo de reacción que catalizan (Nomenclatura EC).
- • Análisis de la Hexoquinasa (Opción 2 – Correcta):
- – Reacción: Glucosa + ATP → Glucosa-6-fosfato + ADP.
- – Acción: Transfiere un grupo funcional (grupo fosforilo, -PO32-) de una molécula donadora (ATP) a una aceptora (Glucosa).
- – Por definición, cualquier enzima que mueve grupos químicos (metilos, fosfatos, aminos) entre moléculas es una Transferasa (EC 2). Las quinasas son un subgrupo de estas.
- • Otras clases:
- – Oxidorreductasas (EC 1): Transfieren electrones (redox). Ej: Deshidrogenasas.
- – Hidrolasas (EC 3): Rompen enlaces usando agua. Ej: Lipasas, peptidasas.
- – Liasas (EC 4): Rompen enlaces sin agua ni oxidación, formando dobles enlaces. Ej: Descarboxilasas.
Pregunta 184
La subunidad Fo de la ATP sintasa mitocondrial:
- 1. Funciona como un canal de electrones.
- 2. Aprovecha la energía de un gradiente de protones a través de la subunidad F1 para sintetizar ATP.
- 3. Cataliza tanto la síntesis como la hidrólisis del ATP.
- 4. Es una proteína integral de la membrana mitocondrial interna.
Explicación:
El Complejo V o ATP Sintasa es un motor molecular compuesto por dos sectores principales: Fo (oligomicina-sensible) y F1.
- • Sector Fo (Opción 4 – Correcta):
- – Es la porción hidrofóbica del complejo.
- – Está incrustada en la bicapa lipídica, actuando como una proteína integral de membrana.
- – Funciona como un canal de protones (no de electrones, Opción 1) que permite el flujo de H+ desde el espacio intermembrana hacia la matriz, impulsando la rotación del tallo.
- • Sector F1 (Contraste):
- – Es la porción periférica hidrofílica que protruye hacia la matriz mitocondrial.
- – Contiene los sitios catalíticos responsables de la síntesis/hidrólisis de ATP (Opción 3).
Pregunta 185
¿Qué afirmación es FALSA en relación con el complejo Piruvato Deshidrogenasa?:
- 1. Cataliza la descarboxilación oxidativa del piruvato.
- 2. Canaliza el piruvato producido en la glicolisis hacía el ciclo de los ácidos tricarboxílicos.
- 3. La reacción que cataliza es reversible en condiciones celulares en mamíferos, lo que permite la síntesis de glucosa a partir de acetil-CoA.
- 4. Está compuesta por múltiples copias de tres enzimas y requiere de cinco coenzimas para catalizar la reacción.
Explicación:
El complejo Piruvato Deshidrogenasa (PDH) es la «puerta de enlace» entre la glucólisis y el ciclo de Krebs.
- • Análisis de la afirmación Falsa (Opción 3 – Correcta):
- – La reacción global es: Piruvato + CoA + NAD+ → Acetil-CoA + CO2 + NADH.
- – Esta reacción es termodinámicamente irreversible en células animales (ΔG muy negativo).
- – Consecuencia metabólica: Los mamíferos no pueden convertir Acetil-CoA (producto de la degradación de ácidos grasos) de nuevo en Piruvato para hacer gluconeogénesis. Por tanto, los ácidos grasos no pueden convertirse en glucosa.
- • Veracidad de las otras opciones:
- – Opción 1 y 2: Correcto, convierte el piruvato (3C) en Acetil-CoA (2C), liberando CO2 y canalizándolo al ciclo de Krebs.
- – Opción 4: Correcto, es un enorme complejo multienzimático (E1, E2, E3) que usa 5 cofactores: TPP, Lipoamida, FAD, NAD+ y Coenzima A.
Pregunta 186
β-Hidroxibutirato y acetoacetato:
- 1. Junto con la acetona, se conocen como cuerpos cetónicos.
- 2. Se sintetizan en el hígado a partir de piruvato.
- 3. Los tejidos extrahepáticos no los pueden metabolizar.
- 4. Su producción disminuye en ayuno prolongado y diabetes no tratada.
Explicación:
Los cuerpos cetónicos son combustibles alternativos solubles en agua producidos por el hígado.
- • Definición (Opción 1 – Correcta):
- – Los tres compuestos son: Acetoacetato, β-hidroxibutirato (el más abundante en sangre) y Acetona (producto de desecho volátil).
- • Errores en las otras opciones:
- – Opción 2: Se sintetizan a partir de Acetil-CoA (derivado principalmente de la oxidación de ácidos grasos), no de piruvato.
- – Opción 3: Precisamente su función es ser exportados a tejidos extrahepáticos (cerebro, corazón, músculo) donde se reconvierten en Acetil-CoA para dar energía. El hígado los produce pero no puede usarlos (carece de la enzima tioforasa).
- – Opción 4: En ayuno y diabetes, la producción aumenta drásticamente (cetosis/cetoacidosis) debido a la movilización masiva de grasas y la falta de glucosa intracelular.
Pregunta 187
Las células que captan colesterol de las lipoproteínas LDL, tienen en su membrana receptores-LDL que reconocen e interactúan ¿Con qué apoproteína?:
- 1. ApoA.
- 2. ApoB100.
- 3. ApoCII.
Explicación:
El receptor de LDL es una proteína de membrana clave para retirar el «colesterol malo» de la circulación mediante endocitosis mediada por receptor.
- • El Ligando Específico (Opción 2 – Correcta):
- – La Apolipoproteína B-100 (ApoB100) es la proteína estructural mayoritaria de las partículas LDL y VLDL.
- – Envuelve la partícula lipídica y posee el dominio de unión que encaja perfectamente en el receptor LDL de las células (hígado y tejidos periféricos).
- – Mutaciones en ApoB100 o en el receptor causan Hipercolesterolemia Familiar.
- • Otras apoproteínas:
- – ApoA (Opción 1): Es la principal proteína de las HDL («colesterol bueno»).
- – ApoCII (Opción 3): Es un cofactor que activa la Lipoproteína Lipasa (LPL) para degradar triglicéridos en sangre, pero no es el ligando principal de endocitosis.
Pregunta 188
En el código genético:
- 1. De los 64 codones de los que consta el código, 61 codifican algún aminoácido.
- 2. Todos los aminoácidos están codificados por más de un codón.
- 3. El codón de inicio (AUG) codifica el aminoácido glicina.
- 4. Hay 2 codones de terminación: UAG y UGA.
Explicación:
El código genético es el diccionario que traduce tripletes de nucleótidos (codones) en aminoácidos.
- • Análisis Numérico (Opción 1 – Correcta):
- – Existen 4 bases (A, U, G, C) agrupadas de 3 en 3: 43 = 64 combinaciones posibles.
- – De estos 64 codones, 3 son de terminación («Stop») y no codifican ningún aminoácido.
- – Por tanto, 64 – 3 = 61 codones que sí codifican aminoácidos.
- • Corrección de errores:
- – Opción 2: Falso. Aunque el código es degenerado, existen dos excepciones: Metionina (AUG) y Triptófano (UGG) tienen un solo codón.
- – Opción 3: El codón de inicio AUG codifica siempre Metionina, no glicina.
- – Opción 4: Hay 3 codones de terminación: UAA («Ocre»), UAG («Ámbar») y UGA («Ópalo»).
Pregunta 189
¿Qué proteínas facilitan el plegamiento de las cadenas polipeptídicas?:
- 1. Carabinas moleculares o chaperonas.
- 2. Ubiquitinas.
- 3. Proteasomas.
- 4. Factores de plegamiento.
Explicación:
Para que una proteína sea funcional, debe adquirir su estructura tridimensional nativa. A menudo, este proceso necesita ayuda para evitar que la proteína se enrede incorrectamente.
- • Las Chaperonas Moleculares (Opción 1 – Correcta):
- – Son una familia de proteínas (ej. Hsp70, Hsp60/GroEL) que se unen a las cadenas polipeptídicas nacientes o mal plegadas.
- – Su función es prevenir la agregación inespecífica y facilitar el plegamiento correcto gastando ATP.
- – Actúan como «acompañantes» (de ahí el nombre francés chaperon) que guían a la proteína hacia su conformación estable.
- • Descarte de las otras opciones:
- – Ubiquitinas (Opción 2): Son pequeñas proteínas que se unen a otras para marcarlas («etiqueta de la muerte») para su degradación.
- – Proteasomas (Opción 3): Son los complejos «trituradores» que degradan las proteínas marcadas con ubiquitina.
Pregunta 190
¿Cuál es la actividad correctora de pruebas de la DNA polimerasa?:
- 1. 5’→3’ Endonucleasa.
- 2. 3’→5’ Endonucleasa.
- 3. 5’→3’ Exonucleasa.
- 4. 3’→5’ Exonucleasa.
Explicación:
La ADN polimerasa tiene una capacidad de autocorrección (proofreading) que reduce la tasa de error durante la replicación de 10-5 a 10-7.
- • Mecanismo de Corrección (Opción 4 – Correcta):
- – La síntesis siempre avanza en dirección 5′ → 3′ (añade nucleótidos al extremo 3′).
- – Si la enzima detecta que ha añadido una base incorrecta, se detiene y retrocede en dirección opuesta (hacia el extremo 5′).
- – Elimina el nucleótido erróneo desde el extremo libre (actividad Exonucleasa) en dirección 3′ → 5′.
- – Es como la tecla «Backspace» (borrar hacia atrás) de un ordenador.
- • Diferenciación de actividades:
- – Exonucleasa 5’→3′ (Opción 3): Elimina nucleótidos «hacia adelante». Es usada por la ADN Polimerasa I para quitar los cebadores de ARN.
- – Endonucleasa (Opciones 1 y 2): Corta el enlace fosfodiéster en el interior de la cadena (no desde los extremos). No es función típica de la polimerasa.
Pregunta 191
¿Por qué muchas proteínas intracelulares NO contienen enlaces disulfuro?:
- 1. Porque los enlaces disulfuro se forman únicamente en ambientes ácidos.
- 2. Porque el medio intracelular es muy oxidante, lo que impide su formación.
- 3. Porque las proteínas intracelulares no requieren estabilidad estructural.
- 4. Porque el medio intracelular es reductor, lo que evita la formación de enlaces—S—S—.
Explicación:
Los enlaces disulfuro (puentes cistina) son enlaces covalentes formados por la oxidación de dos grupos tiol (-SH) de residuos de cisteína.
- • El Ambiente Citosólico (Opción 4 – Correcta):
- – El citosol de la célula es un ambiente fuertemente reductor.
- – Esto se debe a la alta concentración de agentes reductores como el glutatión (GSH) y tiorredoxinas.
- – En estas condiciones, los grupos sulfhidrilo de las cisteínas se mantienen en su forma reducida (-SH), impidiendo termodinámicamente la formación estable de puentes disulfuro (-S-S-).
- • ¿Dónde hay disulfuros entonces?:
- – Son típicos de proteínas extracelulares (secretadas) o de membrana. Se forman en el lumen del Retículo Endoplasmático, que sí posee un ambiente oxidante adecuado para su estabilización.
Pregunta 192
¿Qué papel desempeña el residuo de histidina en la estructura del grupo hemo dentro de la hemoglobina?:
- 1. Oxida al hierro para activar la unión con el oxígeno.
- 2. Estabiliza la forma férrica del hierro una vez que se une al O₂.
- 3. Ocupa uno de los enlaces de coordinación del hierro, ayudando a evitar su oxidación y controlando el acceso del O₂.
- 4. Forma un enlace covalente con el grupo hemo para evitar la liberación del oxígeno.
Explicación:
El hierro (Fe2+) en el grupo hemo puede formar 6 enlaces de coordinación: 4 con los nitrógenos del anillo de porfirina y 2 perpendiculares al plano.
- • Histidina Proximal (F8) y Distal (E7) (Opción 3 – Correcta):
- – La Histidina Proximal ocupa la 5ª posición de coordinación, anclando el grupo hemo a la proteína.
- – La Histidina Distal se sitúa cerca del sitio de unión del ligando (6ª posición). Aunque no se une directamente al hierro, crea un impedimento estérico que fuerza al oxígeno a unirse en ángulo (evitando la oxidación a Fe3+) y dificulta la entrada de moléculas tóxicas lineales como el monóxido de carbono (CO).
- – En conjunto, controlan el microambiente para que la unión sea reversible y segura.
- • Errores en las otras opciones:
- – Opción 1 y 2: El hierro debe mantenerse en estado ferroso (Fe2+). Si se oxida a férrico (Fe3+, metahemoglobina), pierde la capacidad de transportar oxígeno.
Pregunta 193
¿Cuál de las siguientes pruebas es más adecuada para comparar las medias de dos muestras, que poseen ambas distribuciones normales y presentan homogeneidad de varianzas?:
- 1. Mann-Whitney.
- 2. Kruskal-Wallis.
- 3. Friedman.
- 4. t de Student.
Explicación:
La elección del test estadístico depende de tres factores: tipo de variable (cuantitativa), número de grupos (dos) y cumplimiento de supuestos (normalidad y homocedasticidad).
- • Análisis del Caso (Opción 4 – Correcta):
- – Objetivo: Comparar 2 medias.
- – Condiciones: Se cumplen la Normalidad (paramétrico) y la Homocedasticidad (varianzas iguales).
- – Test Indicado: La t de Student para muestras independientes es la prueba paramétrica más potente y adecuada en este escenario ideal.
- • ¿Cuándo usaríamos las otras?:
- – Mann-Whitney (Opción 1): Es la alternativa no paramétrica a la t de Student (cuando NO hay normalidad).
- – Kruskal-Wallis (Opción 2): Alternativa no paramétrica para comparar 3 o más grupos (equivalente al ANOVA).
- – Friedman (Opción 3): Alternativa no paramétrica para medidas repetidas (datos pareados de 3 o más grupos).
Pregunta 194
Para el cálculo de la sensibilidad diagnóstica de una prueba, ¿cuál de las siguientes opciones es necesaria para poder calcular la sensibilidad diagnóstica de una prueba?:
- 1. Verdaderos positivos y falsos positivos.
- 2. Verdaderos negativos y falsos positivos.
- 3. Falsos negativos y verdaderos positivos.
- 4. Falsos negativos y verdaderos negativos.
Explicación:
La sensibilidad mide la capacidad de una prueba para detectar la enfermedad en sujetos que realmente la tienen (tasa de verdaderos positivos).
- • La Fórmula (Opción 3 – Correcta):
- – Matemáticamente: Sensibilidad = VP / (VP + FN).
- – VP (Verdaderos Positivos): Enfermos detectados correctamente.
- – FN (Falsos Negativos): Enfermos que la prueba no detectó (dio negativo erróneamente).
- – El denominador (VP + FN) representa el total de enfermos. Por tanto, para calcularla necesitamos conocer ambos valores.
- • Otras combinaciones:
- – Opción 1 (VP y FP): Se usan para el Valor Predictivo Positivo.
- – Opción 2 (VN y FP): Son los componentes de la columna de «Sanos», necesarios para calcular la Especificidad.
Pregunta 195
¿Cuál de las siguientes es una medida de dispersión estadística?:
- 1. La media geométrica.
- 2. La moda.
- 3. La mediana.
- 4. La varianza.
Explicación:
En estadística descriptiva, distinguimos entre medidas que nos dicen «dónde está el centro» y medidas que nos dicen «cuánto se alejan los datos de ese centro».
- • Medidas de Dispersión (Opción 4 – Correcta):
- – Indican la variabilidad de los datos.
- – La Varianza (S2) mide el promedio de las desviaciones al cuadrado respecto a la media.
- – Otras medidas de dispersión son la Desviación Típica (raíz de la varianza), el Rango y el Rango Intercuartílico.
- • Medidas de Tendencia Central (Opciones 1, 2 y 3):
- – Media (aritmética o geométrica): El promedio.
- – Moda: El valor más frecuente.
- – Mediana: El valor central que divide la distribución en dos mitades iguales.
Pregunta 196
Sobre el coeficiente de correlación de Pearson (ρ) entre dos variables:
- 1. Los valores de ρ se encuentran entre 0 y 1 (0 < ρ < 1).
- 2. Si los valores de ρ se encuentran entre 0 y 1 (0 < ρ < 1) existe una correlación negativa.
- 3. Si ρ > 0, cuando una de las variables aumenta, la otra disminuye.
- 4. Si ρ = 0, no existe correlación lineal entre las variables.
Explicación:
El coeficiente de correlación de Pearson (ρ o r) mide la fuerza y la dirección de la relación lineal entre dos variables cuantitativas.
- • Propiedades Fundamentales (Opción 4 – Correcta):
- – Rango: Oscila siempre entre -1 y +1. (Descarta la Opción 1).
- – Signo: • Positivo (+): Ambas variables aumentan juntas (relación directa). (Descarta las Opciones 2 y 3). • Negativo (-): Cuando una aumenta, la otra disminuye (relación inversa).
- – Valor Cero: Si ρ = 0, los puntos forman una nube dispersa sin tendencia clara, indicando ausencia de relación lineal.
Pregunta 197
Al efectuar un contraste de hipótesis, ¿qué se entiende por error de tipo I?:
- 1. Es el error que se comete cuando la hipótesis nula es rechazada siendo la hipótesis nula verdadera.
- 2. Es el error que se comete si el tamaño de la muestra excede de la potencia estadística del contraste.
- 3. Es el error que se comete cuando la hipótesis nula no es rechazada siendo la hipótesis nula verdadera.
- 4. Es el error que se comete si la hipótesis nula no es rechazada cuando la hipótesis nula es falsa.
Explicación:
En inferencia estadística, siempre corremos el riesgo de equivocarnos al tomar una decisión sobre la Hipótesis Nula (H0).
- • Error Tipo I o α (Falso Positivo) (Opción 1 – Correcta):
- – Ocurre cuando el investigador ve un efecto que no existe.
- – Decisión: Rechazar H0 (decir que hay diferencias).
- – Realidad: H0 es Verdadera (no hay diferencias).
- – Su probabilidad es el nivel de significación (α), habitualmente 0.05.
- • Error Tipo II o β (Falso Negativo) (Opción 4):
- – Ocurre cuando no detectamos un efecto que sí existe. No rechazamos H0 cuando es Falsa.
Pregunta 198
¿Cuál de los siguientes coeficientes estadísticos se utiliza para evaluar la forma de una variable estadística unidimensional?:
- 1. Rango intercuartílico.
- 2. Coeficiente de curtosis de Fisher.
- 3. Coeficiente de correlación de Pearson.
- 4. Mediana.
Explicación:
Para describir completamente una variable, necesitamos medidas de Tendencia Central, Dispersión y Forma.
- • Medidas de Forma (Opción 2 – Correcta):
- – Evalúan la «silueta» del histograma sin importar su centro o su ancho.
- – Curtosis (o apuntamiento): Mide cuán «picuda» es la distribución y el grosor de sus colas respecto a la Normal.
- – Leptocúrtica: Muy apuntada. Platicúrtica: Aplanada.
- – Otra medida de forma es el Coeficiente de Asimetría (Skewness).
- • Otras medidas:
- – Mediana (Opción 4): Posición central.
- – Rango Intercuartílico (Opción 1): Dispersión.
- – Pearson (Opción 3): Relación entre dos variables (bidimensional).
Pregunta 199
En un contraste de hipótesis sobre igualdad de varianzas de 2 poblaciones con distribución normal, ¿qué variable aleatoria se utiliza para resolver el contraste?:
- 1. Chi-cuadrado.
- 2. F de Snedecor.
- 3. t de Student.
- 4. Normal tipificada.
Explicación:
La comparación de la variabilidad (dispersión) entre dos grupos es fundamental antes de aplicar otros tests (homocedasticidad).
-
• El Estadístico F (Opción 2 – Correcta):
- – Para comparar dos varianzas poblacionales (σ12 y σ22), calculamos el cociente de las varianzas muestrales: F = S12 / S22.
- – Si las varianzas son iguales, el cociente debería ser cercano a 1.
- – La distribución de probabilidad que modela este cociente de sumas de cuadrados es la F de Snedecor (también conocida como F de Fisher-Snedecor).
-
• Uso de las otras distribuciones:
- – Chi-cuadrado (χ2): Se usa para inferencias sobre la varianza de una sola población (o para tablas de contingencia).
- – t de Student: Se usa para comparar medias (cuando la varianza es desconocida).
- – Normal (Z): Se usa para comparar medias con muestras muy grandes o varianzas conocidas.
Pregunta 200
En el caso de comparar 2 medias de 2 variables cuyo comportamiento NO es normal, teniendo muestras apareadas y varianzas desconocidas, ¿cuál es el test apropiado?:
- 1. Test de Welch.
- 2. Test de Mcnemar.
- 3. Test de Barlett.
- 4. Test de Wilcoxon.
Explicación:
Para elegir el test estadístico, debemos seguir un árbol de decisión basado en las condiciones de los datos.
-
• Análisis de las condiciones:
- 1. NO Normal: Descarta tests paramétricos (t de Student, Welch). Necesitamos estadística no paramétrica (basada en rangos).
- 2. Muestras apareadas: Los datos vienen en parejas (ej. antes vs. después en el mismo paciente).
-
• Selección del Test (Opción 4 – Correcta):
- – El Test de los rangos con signo de Wilcoxon es la alternativa no paramétrica a la t de Student para muestras apareadas.
- – Evalúa si las diferencias entre los pares tienden a ser positivas o negativas, sin asumir normalidad.
-
• ¿Por qué no los otros?:
- – Test de Welch (Opción 1): Es paramétrico (exige normalidad) y para muestras independientes.
- – Test de McNemar (Opción 2): Es para muestras apareadas, pero de variables cualitativas dicotómicas (Sí/No), no cuantitativas (medias).
- – Test de Bartlett (Opción 3): Sirve para comprobar la igualdad de varianzas (homocedasticidad), no para comparar medias.
Pregunta 201
¿Cuál de estos ligandos es un ligando con una mayor Kd para formar compuestos organometálicos?:
- 1. Cianuro.
- 2. Etilendiamina.
- 3. Etileno.
- 4. Agua.
Explicación:
La constante de disociación (Kd) es inversa a la estabilidad del complejo. Una Kd alta indica un enlace débil (el complejo tiende a romperse), mientras que una Kd baja indica un enlace fuerte.
-
• Análisis de Estabilidad (Opción 3 – Correcta):
- – Cianuro (CN–): Es un ligando de campo fuerte y buen aceptor π. Forma complejos extremadamente estables (Kd muy baja).
- – Etilendiamina: Es un agente quelante. Por el efecto quelato, forma complejos muy estables (Kd muy baja).
- – Etileno (C2H4): Es un ligando π-ácido neutro que se une mediante el modelo Dewar-Chatt-Duncanson. Aunque forma compuestos organometálicos (como la Sal de Zeise), el enlace es generalmente más débil y lábil que el de los cianuros o quelatos. Es común que las olefinas se disocien o intercambien en ciclos catalíticos.
- – Nota: El agua no suele formar enlaces M-C (no organometálicos). Entre las opciones organometálicas (Cianuro y Etileno), el etileno tiene la unión más débil (Mayor Kd).
Pregunta 202
¿Qué se obtiene al adicionar Br2 a un alqueno en presencia de agua?:
- 1. Alcohol.
- 2. Dihaluro.
- 3. Halohidrina.
- 4. Éster.
Explicación:
La reacción sigue un mecanismo de adición electrofílica donde el disolvente participa activamente.
-
• Mecanismo (Opción 3 – Correcta):
- 1. El alqueno ataca al Br2 formando un puente de ion bromonio cíclico intermedio.
- 2. En el segundo paso, se necesita un nucleófilo para abrir el anillo. Aunque hay iones Br– presentes, el agua (el disolvente) es mucho más abundante.
- 3. El agua ataca al carbono más sustituido (apertura anti), introduciendo un grupo -OH tras desprotonarse.
- – El resultado es un compuesto con un halógeno (-X) y un hidroxilo (-OH) en carbonos vecinales: una Halohidrina.
-
• Comparación:
- – Si el disolvente fuera inerte (ej. CCl4), el nucleófilo sería el Br– y se obtendría un Dihaluro vecinal (dibromoalcano).
Pregunta 203
¿Cuál es la respuesta VERDADERA respecto a los métodos ópticos de análisis?:
- 1. Los métodos ópticos de análisis no espectroscópicos se clasifican en métodos de absorción y emisión.
- 2. Los métodos de emisión se basan en la absorción selectiva de radiación.
- 3. La turbidimetría es una técnica analítica espectroscópica basada en la dispersión de la luz.
- 4. La luminiscencia es una técnica analítica espectroscópica basada en la emisión de radiación.
Explicación:
Es importante distinguir entre fenómenos de interacción materia-energía (espectroscopia) y fenómenos de cambio de dirección de la luz (óptica física).
-
• Análisis de la verdad (Opción 4 – Correcta):
- – La Luminiscencia (fluorescencia, fosforescencia) implica que la molécula absorbe energía y luego la emite (se desexcita) liberando fotones. Es, por definición, una técnica espectroscópica de emisión.
-
• Por qué las otras son falsas:
- – Opción 1: Absorción y Emisión son fenómenos cuánticos, por tanto son métodos espectroscópicos, no «no espectroscópicos». (Los no espectroscópicos son refractometría, polarimetría, etc.).
- – Opción 2: Contradicción directa. Los métodos de emisión se basan en la emisión, no en la absorción.
- – Opción 3: La turbidimetría se basa en la dispersión (scattering) de la luz por partículas, no en transiciones de niveles de energía cuántica. Generalmente se clasifica como método óptico no espectroscópico (aunque use un espectrofotómetro para medir).
Pregunta 204
¿Cómo se puede reconocer la materia orgánica fija frente a otra mezcla de cationes inorgánicos en un análisis de un líquido?:
- 1. Al calentar queda un residuo negro, insoluble en ácido.
- 2. Al calentar queda un residuo el cual no arde al calcinar.
- 3. Al añadir NaOH 2M se produce un precipitado rojo.
- 4. Al añadir H2O2 la disolución se torna azul.
Explicación:
En el análisis cualitativo sistemático (marcha analítica), la presencia de materia orgánica puede interferir con la identificación de cationes, por lo que es crucial detectarla y eliminarla.
-
• Ensayo de Carbonización (Opción 1 – Correcta):
- – Los compuestos orgánicos, al ser sometidos a calentamiento fuerte (calcinación), sufren pirólisis.
- – El esqueleto carbonado se descompone dejando un residuo carbonoso de color negro intenso (carbón).
- – Una característica clave para distinguirlo de algunos óxidos metálicos negros (como el de cobre o manganeso) es que el carbón es insoluble en ácidos minerales (HCl, HNO3 diluido), mientras que los óxidos inorgánicos suelen disolverse.
-
• Análisis de las otras opciones:
- – Opción 2: Es característico de las sales inorgánicas estables, que dejan un residuo (blanco o coloreado) que no se quema.
- – Opción 3: Precipitado rojo con NaOH sugiere cationes como Fe3+ (hidróxido férrico), no materia orgánica.
- – Opción 4: El color azul con H2O2 en medio ácido y éter es la prueba específica del Cromo (VI) formando ácido peroxocrómico.
Pregunta 205
¿Cuál es el orden correcto de las etapas en un ciclo de la reacción en cadena de la Polimerasa (PCR)?:
- 1. Elongación → Desnaturalización → Hibridación (Alineamiento).
- 2. Desnaturalización → Alineamiento → Elongación.
- 3. Alineamiento → Elongación → Desnaturalización.
- 4. Elongación → Alineamiento → Desnaturalización.
Explicación:
La PCR es una técnica cíclica que imita la replicación del ADN in vivo, pero utilizando cambios de temperatura para controlar las enzimas y la hibridación.
-
• Las 3 Etapas del Ciclo (Opción 2 – Correcta):
-
1. Desnaturalización (94-98 °C):
Se necesita calor intenso para romper los puentes de hidrógeno y separar la doble hélice de ADN en dos cadenas sencillas (molde). Es el paso inicial obligatorio para exponer la secuencia. -
2. Alineamiento / Hibridación (Annealing) (50-65 °C):
Se baja la temperatura para permitir que los cebadores (primers) se unan específicamente a sus secuencias complementarias en las cadenas molde. -
3. Elongación / Extensión (72 °C):
Se sube la temperatura al punto óptimo de funcionamiento de la ADN polimerasa (Taq polimerasa), que sintetiza la nueva cadena complementaria añadiendo dNTPs a partir de los cebadores.
-
1. Desnaturalización (94-98 °C):
Pregunta 206
En condiciones de hipoxia tisular, la hemoglobina S sufre una transición conformacional que favorece su agregación. ¿Cuál de los siguientes factores contribuye directamente a esta agregación en los eritrocitos de pacientes homocigotos?:
- 1. La disminución de la constante dieléctrica intracelular, que potencia las interacciones iónicas entre cadenas.
- 2. El desplazamiento del equilibrio tautomerico de la histidina proximal, que desestabiliza la unión al oxígeno.
- 3. La exposición del residuo de valina en la posición 6 de la cadena beta, que facilita interacciones hidrofóbicas inter tetraméricas.
- 4. El incremento en la concentración de 2,3-BPG, que promueve la formación de enlaces cruzados entre grupos hemo.
Explicación:
La anemia falciforme es el ejemplo clásico de una enfermedad molecular causada por una única mutación puntual.
-
• La Mutación y el Efecto Hidrofóbico (Opción 3 – Correcta):
- – En la HbS, el Glutamato (polar/carga negativa) en la posición 6 de la cadena β es sustituido por Valina (apolar/hidrofóbica).
- – En condiciones de oxigenación (Oxi-Hb), este residuo está oculto. Pero en hipoxia (Desoxi-Hb), la proteína cambia de conformación (estado T) y expone este «parche pegajoso» hidrofóbico al exterior.
- – La valina de una molécula encaja en un bolsillo hidrofóbico (formado por Fenilalanina 85 y Leucina 88) de otra molécula de HbS vecina. Esto desencadena una polimerización en cadena, formando fibras largas que deforman el eritrocito (forma de hoz).
-
• Análisis de distractores:
- – Opción 1: La constante dieléctrica del citosol no cambia drásticamente; el problema es hidrofóbico, no electrostático.
- – Opción 4: El 2,3-BPG estabiliza la forma desoxi, pero no crea enlaces cruzados covalentes entre grupos hemo.
Pregunta 207
Cuando se estudia una cinética de reacción, si se representa (1/Concentración) frente al tiempo y se obtiene una línea recta esto indica:
- 1. Que la reacción es de orden 0.
- 2. Que la reacción es de orden 1.
- 3. Que la reacción es de orden 2.
- 4. Esa representación no puede dar una línea recta.
Explicación:
Para determinar el orden de una reacción, utilizamos las ecuaciones de velocidad integradas, que tienen la forma de una recta y = mx + n.
-
• Orden 2 (Opción 3 – Correcta):
- – Ley de velocidad: v = k[A]2.
- – Ecuación integrada: 1/[A] = kt + 1/[A]0.
- – Si representamos 1/[A] (eje Y) frente al tiempo (eje X), obtenemos una recta con pendiente positiva (+k).
-
• Comparación con otros órdenes:
- – Orden 0: Recta al representar [A] vs t. (Pendiente -k).
- – Orden 1: Recta al representar ln[A] vs t. (Pendiente -k).
Pregunta 208
¿Cuál es la relación de isomería entre (2R,3R)-2,3-diclorobutano y (2S,3S)-2,3-diclorobutano?:
- 1. Son enantiómeros.
- 2. Son isómeros funcionales.
- 3. Son isómeros de posición.
- 4. Son diastereoisómeros.
Explicación:
Para clasificar la relación entre estereoisómeros, debemos observar qué ocurre con la configuración absoluta de todos sus centros quirales.
-
• Enantiómeros (Opción 1 – Correcta):
- – Definición: Son imágenes especulares no superponibles.
- – Regla: Se invierten todos los centros quirales.
- – En este caso: El carbono 2 pasa de R → S y el carbono 3 pasa de R → S. Al invertirse ambos, las moléculas son enantiómeras entre sí.
-
• Diastereoisómeros (Opción 4):
- – Ocurre cuando se invierten algunos centros, pero no todos.
- – Ejemplo: Comparar (2R,3R) con (2R,3S). Este último sería el compuesto meso (inactivo ópticamente por plano de simetría interna).
Pregunta 209
¿Qué forma presenta la especie ICl4– ?:
- 1. Plano-cuadrada.
- 2. Octaédrica.
- 3. Balancín o silla de montar.
- 4. Bipirámide trigonal.
Explicación:
Para determinar la geometría, aplicamos la Teoría de Repulsión de Pares de Electrones de la Capa de Valencia (TRPECV o VSEPR).
-
• Recuento de electrones:
- – Yodo (Central): Grupo 17 → 7 electrones de valencia.
- – 4 Cloros (Ligandos): Aportan 1 electrón cada uno → 4 electrones.
- – Carga negativa (-): Sumamos 1 electrón extra.
- – Total: 7 + 4 + 1 = 12 electrones → 6 pares de electrones alrededor del Yodo.
-
• Determinación de la Estructura (Opción 1 – Correcta):
- – Geometría Electrónica: Con 6 pares, la disposición base es Octaédrica.
- – Pares Enlazantes vs. Solitarios: Hay 4 enlaces (I-Cl) y sobran 2 pares (6 – 4 = 2 pares solitarios). Fórmula VSEPR: AX4E2.
- – Geometría Molecular: Para minimizar la repulsión, los dos pares solitarios se colocan en posiciones opuestas (axiales, a 180º). Esto deja a los 4 cloros en el plano ecuatorial formando un cuadrado.
Pregunta 210
Sobre los equilibrios de formación de complejos señale la respuesta FALSA:
- 1. Las constantes de equilibrio de las reacciones de formación de complejos son constantes de formación.
- 2. La constante de formación global de un complejo MLn es el producto de las constantes de formación sucesivas de cada una de las etapas que llevan a la formación de dicho complejo.
- 3. Si un ligando es protonable la concentración de ligando libre no se afecta por el pH.
- 4. Las constantes condicionales de formación de complejos son útiles para tener en cuenta el efecto del pH en la concentración libre de un ligando protonable.
Explicación:
La química de coordinación en solución acuosa está fuertemente influenciada por reacciones secundarias, especialmente las ácido-base.
-
• Análisis de la Falsedad (Opción 3 – Correcta):
- – La mayoría de los ligandos (ej. Amoniaco, Cianuro, EDTA) son Bases de Lewis y también bases de Brønsted.
- – Si el ligando (L) es protonable, existe un equilibrio competitivo: L + H+ ↔ HL+.
- – Al bajar el pH (aumentar H+), el equilibrio se desplaza hacia la forma protonada (HL+), disminuyendo drásticamente la concentración de ligando libre [L] disponible para unirse al metal.
- – Por tanto, la afirmación de que «no se afecta» es totalmente falsa. El pH es la variable más crítica en complexometría.
-
• Veracidad de las otras:
- – Opción 2: Correcto. La constante global (βn) es igual a K1 · K2 · … · Kn.
- – Opción 4: Correcto. Usamos la «Constante Condicional» (K’) que incorpora el coeficiente αL para ajustar la constante termodinámica al pH de trabajo real.